马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?注册
×
概要
作者提出两例锯齿前路游离筋膜瓣联合血管化肩胛骨移植重建创伤性背侧手和指骨骨缺损。具有单个血管蒂的复合皮瓣允许保护严重受伤的手指并提供良好的功能和美容效果。
关键词:肩胛筋膜,肩胛骨,游离皮瓣,手指重建
介绍
伴随手指骨缺损的组织损失对于重建来说是一个具有挑战性的问题。由于骨骼重建和软组织覆盖是强制性的,以挽救手指,原始皮肤表面重修和分期骨移植是治疗的选择。然而,这些方法偶尔会延长治疗期,从而增加关节挛缩的风险。对于包括指骨在内的背部手指缺损的重建,良好血管化的骨骼和薄的,柔韧的软组织是功能和美容观点的理想材料。骨皮瓣可同时提供两种元素,但有时需要脱脂程序。作者提出了一种包括锯齿状前筋膜和肩胛骨的组合瓣,用单个血管蒂满足这些要求,无需额外手术(图1)。
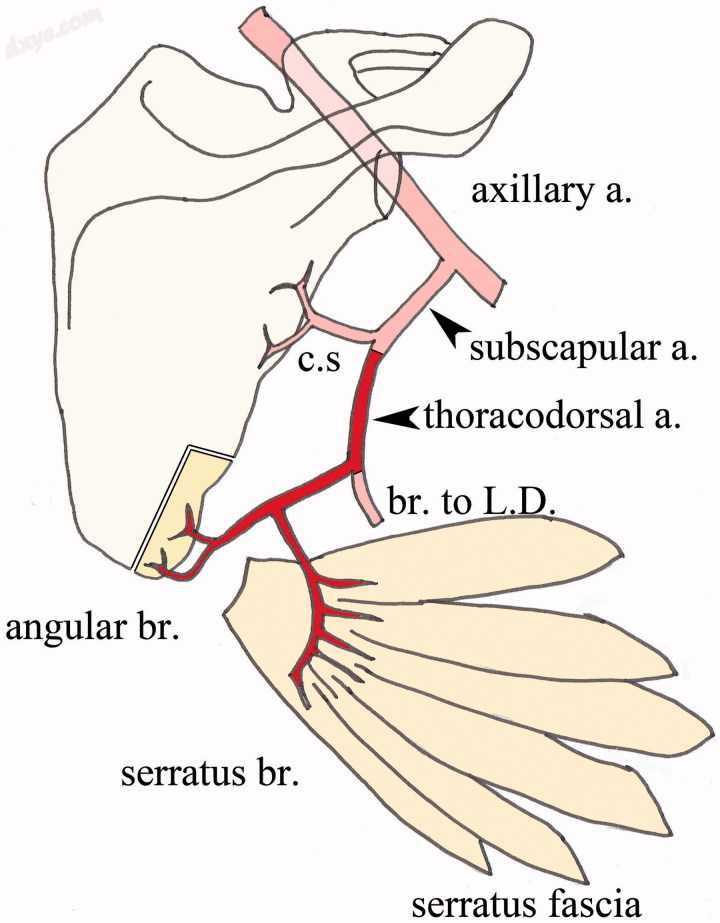
图1。
皮瓣的示意图。
手术程序
从对侧未受伤的一侧采集皮瓣。将患者置于患侧的半侧位置,使未受累的手臂抬高并支撑,并将受伤的手放在手台上。从腋窝褶皱到第八或第九肋骨的水平形成锯齿形切口,并识别背阔肌的外侧和前侧边缘。背阔肌和锯齿前肌之间的平面被发展为暴露维管束和沿着锯齿前肌表面延伸的长胸神经。乳晕组织必须与锯齿肌保持一致,而不是与背阔肌保持一致。胸背动脉的解剖以逆行方式继续至其在肩胛下分叉处的起源。遇到并结扎到背阔肌的分支,并将有角分支解剖到肩胛骨的外侧边缘,然后保存。在将血管蒂移动到所需长度后,将所需尺寸的锯齿状筋膜和覆盖的乳晕组织从腹侧向背侧提升离开肌肉。
长胸神经与筋膜小心分离,但下三个肌肉条的分支被切开并用筋膜抬高,因为允许收集下三条锯齿带作为肌瓣,以防止肩胛骨萎缩[1] ]。根据受体部位要求,来自肩胛骨外侧边界的一段骨骼在附着的肩胛下肌上勾画出轮廓。在沿着标记分割肌纤维以暴露骨表面之后,用振荡锯进行截骨术。使用包含脉管系统到骨骼的小肌肉箍采集骨瓣。
瓣的蒂与解剖鼻烟窝区域中的桡动脉吻合。 将带血管的骨置于指骨缺损中并用手术线固定。 放置锯齿状筋膜以覆盖暴露的骨骼和关节。 分层厚度的皮肤移植物同时进行,没有结扎固定。
病例报告
情况1
一名53岁的男子在机动车撞车事故中右手受伤,仅在远端手背部和中指和无名指上维持复合伤口。 更具体地说,他患有无名指的近节指骨的粉碎性关节内骨折,其具有6×8cm的覆盖软组织缺损,其还包括远端手和中指至近端指间(PIP)关节水平。 无名指的伸肌腱被破坏,但没有丢失(图2)。 右手的掌侧表面保持完整。
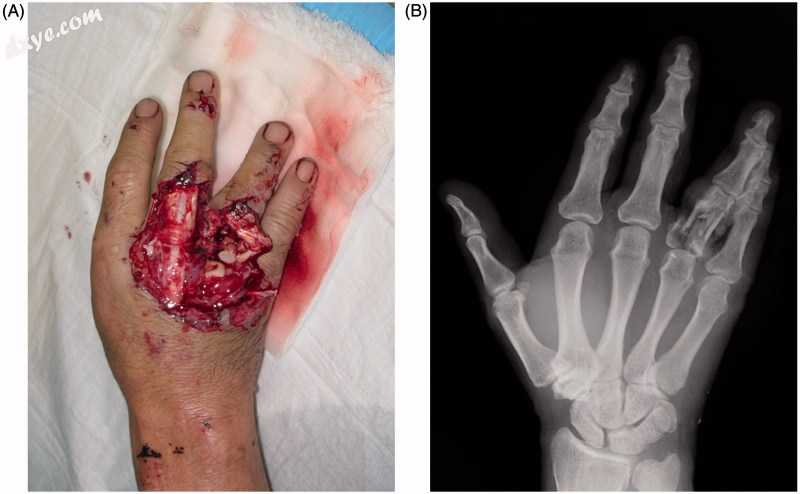
图2。
案例1:初步演示的右手。 (A)显示皮肤缺陷的背视图。 (B)X射线显示环近端指骨的粉碎性骨折。
用人造真皮暂时覆盖伤口,并在损伤后14天进行重建。在外科清创术后,同时采集8×8cm的serratus筋膜区域和距胸背动脉角分支上的肩胛骨3×1×0.5cm的骨块(图3)。膜分支起源于胸背动脉的前锯肌,切除至肩胛下动脉分叉的蒂长度为8 cm。将采集的骨块置于缺损中并缝合破坏的肌腱后,在伤口上放置筋膜瓣。在同一手术区域的同侧胸壁上的分层皮肤移植物被移植到筋膜瓣上。在解剖鼻烟窝中,皮瓣的动脉与桡动脉吻合,皮瓣的静脉以端对端的方式与头静脉吻合。
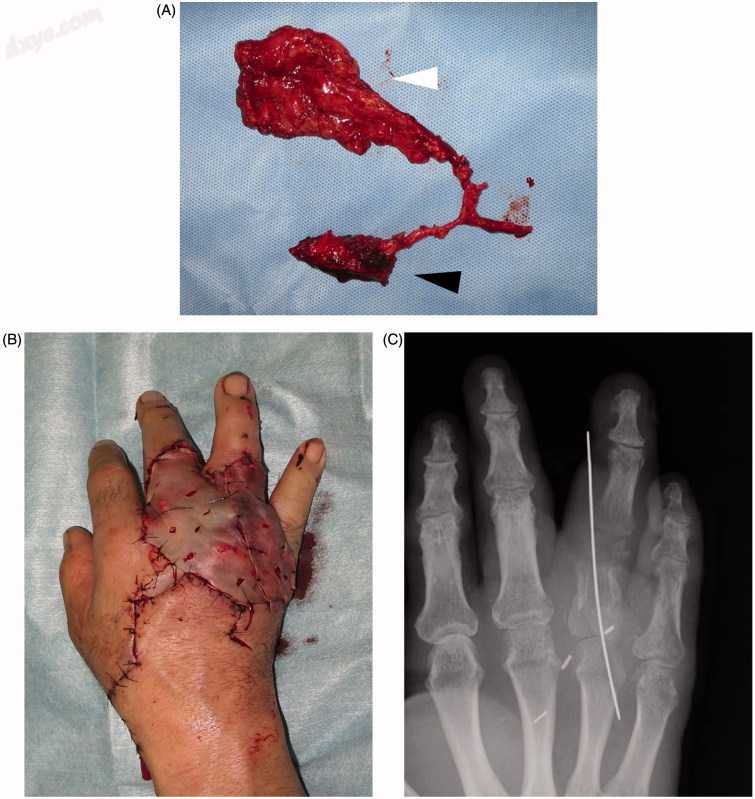
图3。
病例1中的术中发现。(A)采集的皮瓣包括锯齿状前筋膜和带有胸背动脉血管化的肩胛骨。 白色箭头表示筋膜成分,黑色箭头表示骨段。 (B)设置皮瓣,同时进行分层皮肤移植。 (C)立即术后X射线显示无名指的骨骼重建。
缺陷以良好的轮廓重建,而无名指的关节是僵硬的。 术后6个月,掌指关节(MP)关节在40°屈曲时僵硬,PIP和远端指间关节(DIP)关节僵硬。 右手握力为11公斤,左手握力为53公斤。 然而,由于僵硬的手指不会妨碍挤压或抓握,患者不需要额外的手术来改善无名指的运动范围(图4)。
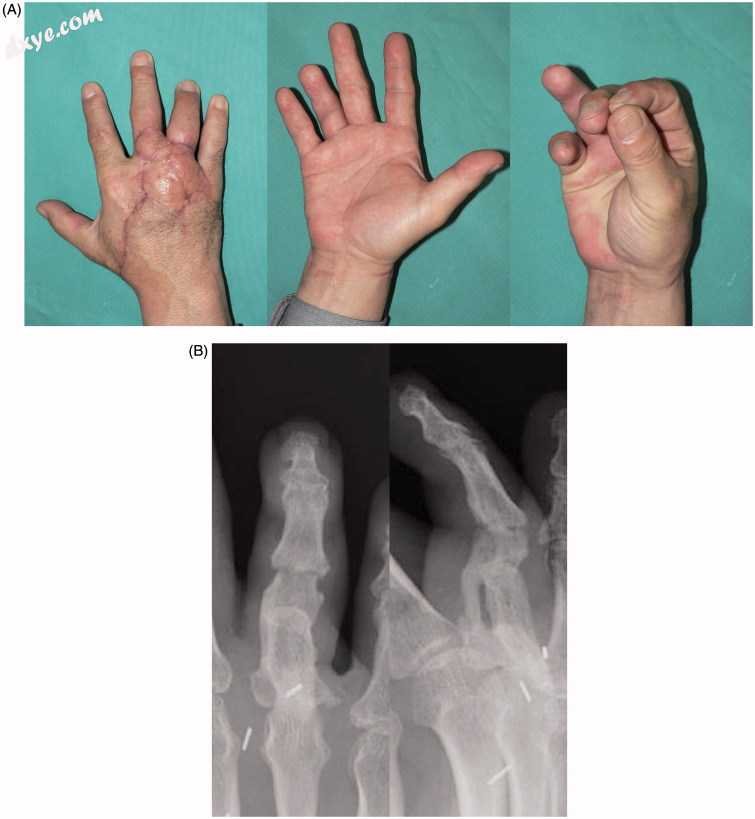
图4。
术后8个月出现病例1。 (A)右手的背侧和掌侧视图。 (B)在X射线上显示的骨愈合。 正面和侧面视图。
案例2
一名36岁的男子在工业事故中左手食指受伤,导致复合组织问题。 他对近端和中间趾骨进行了广泛的粉碎,导致骨丢失和PIP关节闭塞。 此外,上覆的伸肌机制和皮肤无法挽救。 幸运的是,屈肌腱,神经血管束和远端指骨相对较少(图5)。 进行克氏针骨间钉扎以防止由于伤口收缩导致的手指缩短,并且软组织缺陷在同一天暂时被人造真皮取代(图6)。
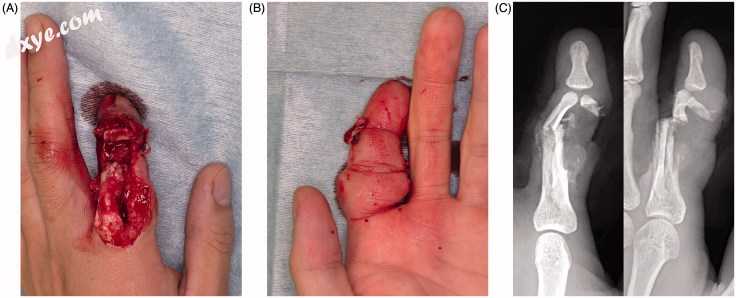
图5。
案例2:左手食指初始演示。 (A)显示皮肤缺损和开放性骨折的背视图。 (B)手指的掌部位保持完整。 (C)描绘粉碎性骨折的X射线。 正面和侧面视图。
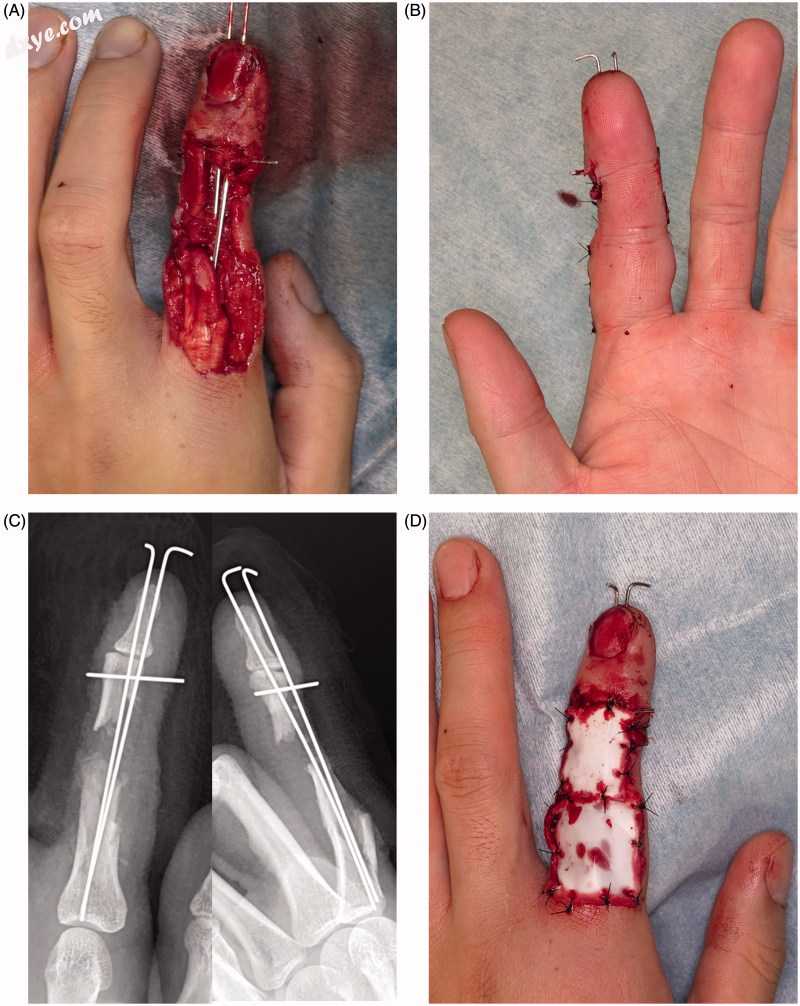
图6。
案例2中的第一次操作。(A)残余骨片的线固定。膨胀罩的缺陷是显而易见的。 (B)通过固定保存食指的原始长度。 (C)描绘骨缺损的X射线。 (D)人造真皮暂时用于覆盖伤口。
在损伤后17天进行重建手术。去除人工真皮后,用胸背动脉抬高6×8cm的锯齿状筋膜面积和4×1×0.7cm的肩胛骨骨段。角分支起源于胸背动脉的前锯肌。将骨块置于近端和中间趾骨的残余骨碎片之间,所有骨碎片均用克氏针和不锈钢丝牢固固定。考虑到损伤的复杂性,利用单块骨骼提供比原始长度短1厘米的固体构造,以允许患者进行三脚架夹伤。暴露的骨头覆盖有锯齿状筋膜。通过胸背动脉到桡动脉的端对端吻合,以及解剖鼻烟窝中的头静脉到头静脉,将皮瓣血运重建。在没有任何压迫的情况下同时施加分层厚度的皮肤移植物在锯齿状筋膜上(图7)。
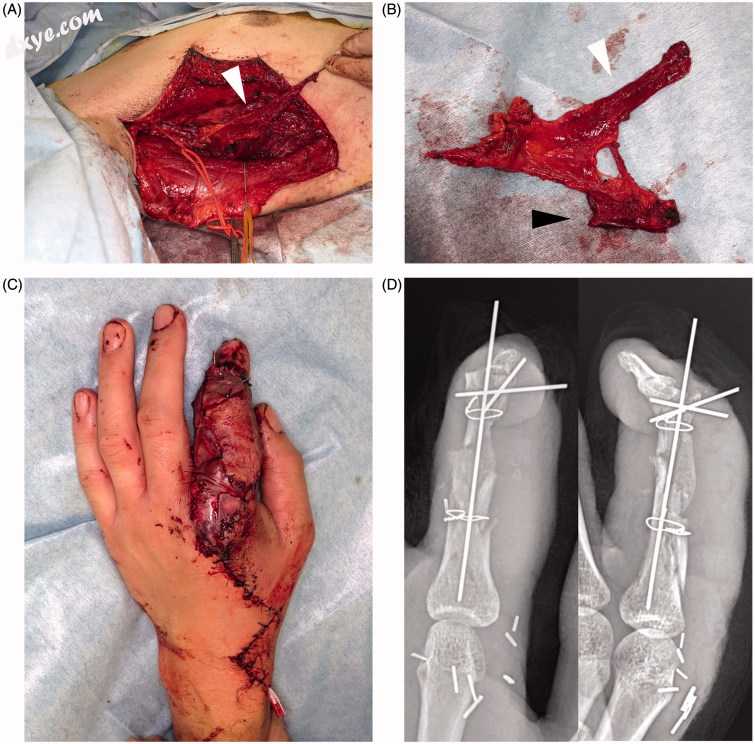
图7。
病例2的第二次手术。(A)皮瓣采集术的术中观察。 白色箭头表示筋膜瓣。 (B)皮瓣的一般视图。 白色箭头表示筋膜成分,黑色箭头表示骨段。 (C)显微外科手术后转移皮瓣,立即分层皮肤移植。 (D)显示用手术线固定的血管化骨移植的食指骨骼重建的X射线。
术后过程很顺利。 尽管重建的手指变得比作者预期的更薄并且PIP关节丢失,但患者获得了MP关节的0/65°的运动范围(图8)。 他在术后6个月没有遇到任何困难就恢复了原来的工作。 他总是试图用挽救的手指抓住或捏,但有时选择不使用食指而是用习惯代替中指。
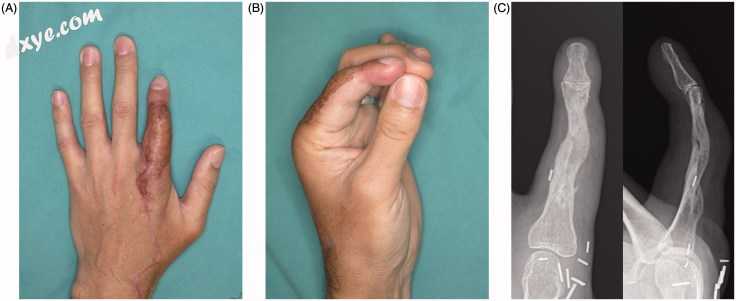
图8。
术后7个月出现病例2。 (A)左手的一般视图。重建的手指萎缩。 (B)缩短食指可以使三脚架收缩。 (C)X射线显示移植骨的结合。
讨论
由于作者的两例患者出现了指骨缺损和背侧皮肤的上部缺损,因此必须采用骨骼支撑和软组织进行重修,以保护受影响的手指。对于骨重建,血管化骨移植优于非血管化骨移植以维持手指长度和强度,因为内源性血液供应导致高抗感染能力[2],并且预期骨吸收最小化。由于美容和功能原因,骨移植物上的软组织覆盖必须薄且柔韧。
骨皮瓣提供了一种有用的重建工具,如游离腓骨皮瓣,肩胛骨或肩胛骨皮瓣和侧臂皮瓣[3]。作者治疗的伤口不需要长骨移植,并且长度不需要腓骨瓣,并且两名患者的下肢非常多毛,并且不适合背部皮肤重修。通常,肩胛骨或肩胛骨瓣的皮瓣对于手指的背面来说太厚,并且侧臂皮瓣在上臂上留下难看的疤痕,当穿着短袖衬衫时这些疤痕容易看见。此外,根据Parrett等人的回顾性研究。 [4],在背部手部重建的美学效果方面,皮肤移植的筋膜皮瓣优于筋膜皮瓣或皮瓣移植皮瓣。参考该研究,作者试图确定可以与血管化骨一起采集的最佳筋膜瓣。
在筋膜皮瓣的类别中,颞顶筋膜皮瓣提供了良好的肌腱滑动材料的好处,同时还提供背部手部覆盖[5,6],并且当伴有颅骨时可能形成骨筋膜瓣[7]。然而,采集颞顶皮瓣会在一些短发患者身上留下难以辨认的疤痕。
首先将锯齿状筋膜皮瓣描述为肌腱滑动材料,用于覆盖Wintsch和Helaly [8]在前臂或腕部水平暴露的屈肌腱。由于其薄,长而恒定的血管蒂,以及供体部位发病率低,这种皮瓣因此与皮肤移植物一起经常应用于背部手部覆盖[9-14]。在这两种情况下,滋养肩胛骨下部的角形分支起源于胸背动脉的锯齿状前分支。根据Seneviratne等人的说法。 [15],仅在25%的解剖中观察到相同的分支模式。超过半数的标本可见背阔肌肌蒂分支。但是,Seitz等人。 [16]注意到有角分支主要来自锯齿分支(48.5%的尸体解剖)。无论哪种方式,筋膜和骨骼之间的蒂的独立性有利于皮瓣定位。
正如几位作者所提到的,由于大量的动脉和静脉分支进入锯齿肌,因此从筋膜提升筋膜时必须进行细致的止血[9,11-14]。塞茨等人。 [17]建议使用超声刀片代替双极凝固器采集锯齿状筋膜瓣。作者使用Harmonic SYNERGY弯曲刀片(Ethicon Endo-Surgery,Cincinnati,OH)并确认其实用性。
serratus筋膜瓣的一个缺点是没有监测皮肤桨。覆盖在锯齿上的皮肤的血液供应由肌肉的不一致的穿支提供,并且更主要地由后第六和第七肋间血管的外侧皮肤分支的穿支提供[18]。作者在术中找不到任何从锯齿到上覆胸部皮肤的穿支,并且发现将皮瓣连接到筋膜上作为监测皮瓣是不可行的。用小肌肉袖带收割皮瓣作为监测组织可能是一个不错的选择。
作者期望锯齿状筋膜在病例1中起到伸肌的滑动表面的作用,但无法证实这一点,因为所涉及关节的功能丧失了。 然而,在不需要皮瓣切除的情况下获得足够薄的手指外观。
考虑到手的功能结果,当其他手指完整时保留单个受损手指可能是有争议的。 然而,一项研究得出结论,与单位屈肌2区截肢再植相比,翻修截肢并不能提供更好的功能结果[19]。 在目前的情况下,拯救严重受损的手指不能完全恢复手部功能,但恢复的手在日常生活中证明是有用的。 患者报告对功能和美容效果总体满意。
参考:
Free serratus anterior fascial flap combined with vascularized scapular bone for reconstruction of dorsal hand and finger defects
1. Whitney TM, Buncke HJ, Alpert BS, et al. The serratus anterior free-muscle flap: experience with 100 consecutive cases. Plast Reconstr Surg. 1990;86:481–490. [PubMed] [Google Scholar]
2. Adani R, Delcroix L, Innocenti M, et al. Reconstruction of large posttraumatic skeletal defects of the forearm by a vascularized free fibular graft. Microsurgery. 2004;24:423–429. [PubMed] [Google Scholar]
3. Kremer T, Bickert B, Germann G, et al. Outcome assessment after reconstruction of complex defects of the forearm and hand with osteocutaneous free flaps. 2006;118:443–454. [PubMed] [Google Scholar]
4. Parrett BM, Bou-Merhi JS, Buntic RF, et al. Refining outcomes in dorsal hand coverage: consideration of aesthetics and donor-site morbidity. Plast Reconstr Surg. 2010;126:1630–1630. [PubMed] [Google Scholar]
5. Brent B, Upton J, Acland RD, et al. Experience with the temporoparietal fascial free flap. Prast Reconstr Surg. 1985;76:177–188. [PubMed] [Google Scholar]
6. Hing DN, Buncke HJ, Alpert BS. Use of the temporoparietal free fascial flap in the upper extremity. Plast Reconstr Surg. 1988;81:534–544. [PubMed] [Google Scholar]
7. Davison SP, Mesbahi AN, Clemens MW, et al. Vascularized calvarial bone flaps and midface reconstruction. Plast Reconstr Surg. 2008;122:10e–18e. [PubMed] [Google Scholar]
8. Wintsch K, Helaly P. Free flap of gliding tissue. J Reconstr Microsurg. 1986;2:143–151. [PubMed] [Google Scholar]
9. Meland BN, Weimar R. Microsurgical reconstruction: experience with free fascia flaps. Ann Plast Surg. 1991;27:1–8. [PubMed] [Google Scholar]
10. Schwabegger AH, Hussl H, Rainer C, et al. Clinical experience and indications of the free serratus fascia flap: a report of 21cases. Plast Reconstr Surg. 1998;102:1939–1946. [PubMed] [Google Scholar]
11. Buehler MJ, Pacelli L, Wilson KM. Serratus fascia “sandwich” free-tissue transfer for complex dorsal hand and wrist avulsion injuries. J Reconstr Microsurg. 1999;15:315–320. [PubMed] [Google Scholar]
12. Fassio E, Laulan J, Aboumoussa J, et al. Serratus anterior free fascial flap for dorsal hand coverage. Ann Plast Surg. 1999;43:77–82. [PubMed] [Google Scholar]
13. Ulrich D, Fuchs P, Bozkurt A, et al. Free serratus anterior fascia flap for reconstruction of hand and finger defects. Arch Orthop Trauma Surg. 2010;130:217–222. [PubMed] [Google Scholar]
14. Fotopoulos P, Holmer P, Leicht P, et al. Dorsal hand coverage with free serratus fascial flap. J Reconstr Microsurg. 2003;19:555–559. [PubMed] [Google Scholar]
15. Seneviratne S, Duong C, Taylor GI. The angular branch of the thoracodorsal artery and its blood supply to the inferior angle of the scapula: an anatomical study. Prast Reconstr Surg. 1999;104:85–88. [PubMed] [Google Scholar]
16. Seitz A, Papp S, Papp C, et al. The anatomy of the angular branch of the thoracodorsal artery. Cells Tissues Org. 1999;164:227–236. [PubMed] [Google Scholar]
17. Seitz IA, Williams C, Schechter LS. Facilitating harvest of the serratus fascial flap with ultrasonic dissection. ePlasty. 2010;10:152–157. [PMC free article] [PubMed] [Google Scholar]
18. Palmer JH, Taylor GI. The vascular territories of the anterior chest wall. Br J Plast Surg. 1986;39:287–299. [PubMed] [Google Scholar]
19. El-Diway M, Odobescu A, Belanger-Douet M, et al. Replantan vs revision amputation in single digit zone II amputations. J Plast Reconstr Aesthet. 2015;68:859–863. [PubMed] [Google Scholar] |


