马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?注册
×
概要
局部切除胃是预防术后症状的理想方法。存在各种进行局部切除的手术,例如腹腔镜病变提升方法,非接触病变提升方法,内窥镜全层切除术和腹腔镜内窥镜合作手术。在内窥镜粘膜下剥离的发明和广泛使用之后,局部切除已经过时作为胃癌的治愈性手术技术。尽管如此,胃癌的局部切除治疗现在有望在临床上使用前哨淋巴结导航手术卷土重来。然而,除正常适应症外,还有许多与胃癌局部切除相关的问题。这些包括胃变形,功能障碍,确保安全的手术切缘,诱导腹膜传播的可能性,以及相关的异时胃癌风险的增加。鉴于这些问题,有一种趋势是将局部切除作为一种调查治疗,仅适用于精心挑选的病例。用于胃癌局部切除胃的理想模型是使用ESD装置进行内窥镜全层胃切除术和使用腹腔镜或手术机器人手动缝合闭合的组合,以实现肿瘤学安全性和保留功能。
关键词:胃癌,局部切除术,腹腔镜内镜下合作手术,前哨淋巴结
介绍
癌症手术中的淋巴结清扫很重要,因为它通常提供准确的分期信息[1]。在某些癌症中,淋巴结清扫也在改善生存结果中起作用。转移局限于局部淋巴结的胃癌,胃切除术的标准淋巴结清扫范围达到D2,治疗效果良好[2,3]。因此,接受D2淋巴结切除治疗胃癌的患者需要广泛的胃切除术,包括远端部分胃切除术或全胃切除术。已知各种胃切除术后症状在这些手术后常规发生[4]。空肠袋插入和其他此类创新性重建方法的益处,作为预防这些症状的措施,仍有待最终证实。有效的对策是减少胃切除术的范围。部分减少D2淋巴结清扫的程度可以减少胃切除的程度。作为有限的手术,日本胃癌治疗指南[5]提到保留幽门的胃切除术,其保留幽门并省略沿右胃动脉的数字'5'淋巴结清扫,以及保留远端胃的近端胃切除术并省略解剖数​​字'4d','5'和'6'淋巴结。尽管这些手术减轻了相对于标准手术的术后症状,但他们未能消除它们[6,7]。因此,局部切除仅局限于存在胃癌并且省略淋巴结清扫的部位,因此是预防术后症状的理想手术策略。
“局部切除胃”是指涉及胃壁的一部分的全厚度局部切除的外科手术。它是“楔形切除术”的同义词。然而,该术语不适用于包括幽门或贲门的切除术。胃沿其短轴的环状切除称为节段性胃切除术,不应与局部切除术混淆。
本文回顾了局部切除胃的适应症和手术方法,并对胃癌的治疗方法进行了展望。
胃癌局部切除的适应症:适应症和目前的概念
仅在没有淋巴结转移的情况下考虑局部胃切除,因此消除了对淋巴结切除的需要并且导致胃的血管供应保持不变。然而,由于胃癌在东亚非常普遍,因此对淋巴结转移的临床病理基础进行了广泛的研究,从而可以对胃癌转移阴性的胃癌病例进行可靠的术前鉴定。
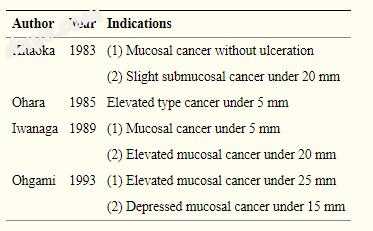
自二十世纪末以来,专门从事胃癌治疗的中心常规进行胃部局部切除术治疗早期胃癌。虽然对胃局部切除的适应症有不同意见,但对小粘膜胃癌的使用存在共识[8-11]。表1显示了胃癌局部切除的代表性适应症。这些适应症基于每个中心在没有淋巴结转移的情况下切除早期胃癌的经验。在具有腹腔镜能力的中心也尝试了腹腔镜局部切除胃。 Ohgami等人。 [11]开发了一种病变解除方法,由于其简单性而赢得了普及。
表格1
在相关的日本文章中提供了进行局部切除的旧指征
然而,随着内镜治疗的出现,胃癌的治疗方法发生了巨大变化。随着内镜下黏膜切除术(EMR)的发展,第一次重大变化。 EMR被描述为使用高频圈套切除胃粘膜的方法[12]。 EMR比手术局部切除胃有优势。首先,它不需要全身麻醉,因此也可以在不适合麻醉的患者中进行。其次,成功的EMR可以保留整个胃,因此这些患者没有任何胃切除术后的症状。然而,执行EMR的技术难度和局部残留病变率(10-35%)是其主要缺点[13]。因此,许多外科医生认为EMR是替代治疗而非标准治疗,导致管理策略不一致,并且在任何特定病例中EMR和腹腔镜局部胃切除之间的选择缺乏清晰度。第二个重要变化是内镜黏膜下剥离术(ESD)的出现[13]。由Hosokawa等人开发。作为EMR的改进方法,ESD涉及使用通过胃镜的钳子通道插入的高频装置,以产生具有宽边缘的环形粘膜切口,然后进行粘膜下剥离,从而实现病变的整块切除。 。与EMR不同,ESD提供可靠的同时切除,具有广泛的边缘,因此与准确的病理诊断和低残留疾病率的优点相关联。根据两个高容量中心的经验和包括5000例手术切除的病例,在病变中表明淋巴结转移阳性的可能性低于手术死亡率[14]。 ESD的适应症包括:(1)无溃疡的分化粘膜癌,(2)3 cm或更小的分化粘膜癌,伴有溃疡瘢痕,(3)分类为SM1的分化癌,3 cm或更小,( 4)未分化的粘膜癌,2厘米或更小,无溃疡。这些是广泛的适应症,包括所有先前报道的手术局部切除胃的指征。可持续发展教育已广泛普及,在切除困难的情况下取得了成功,并且也显示出有利的结果[15]。因此,所有对淋巴结转移呈阴性的早期胃癌都被认为是ESD,不需要局部切除胃以治疗胃癌。
目前局部切除胃的程序
腹腔镜局部切除术
自Ohgami等人对病变提升方法的描述以来,腹腔镜局部切除越来越多。[11]。 病变提升方法是开创性的,因为使用线性吻合器同时进行病变切除和胃壁缝合。 图1总结了病变提升方法的技术。 这是一种简单的技术,但其应用仅限于小病变。
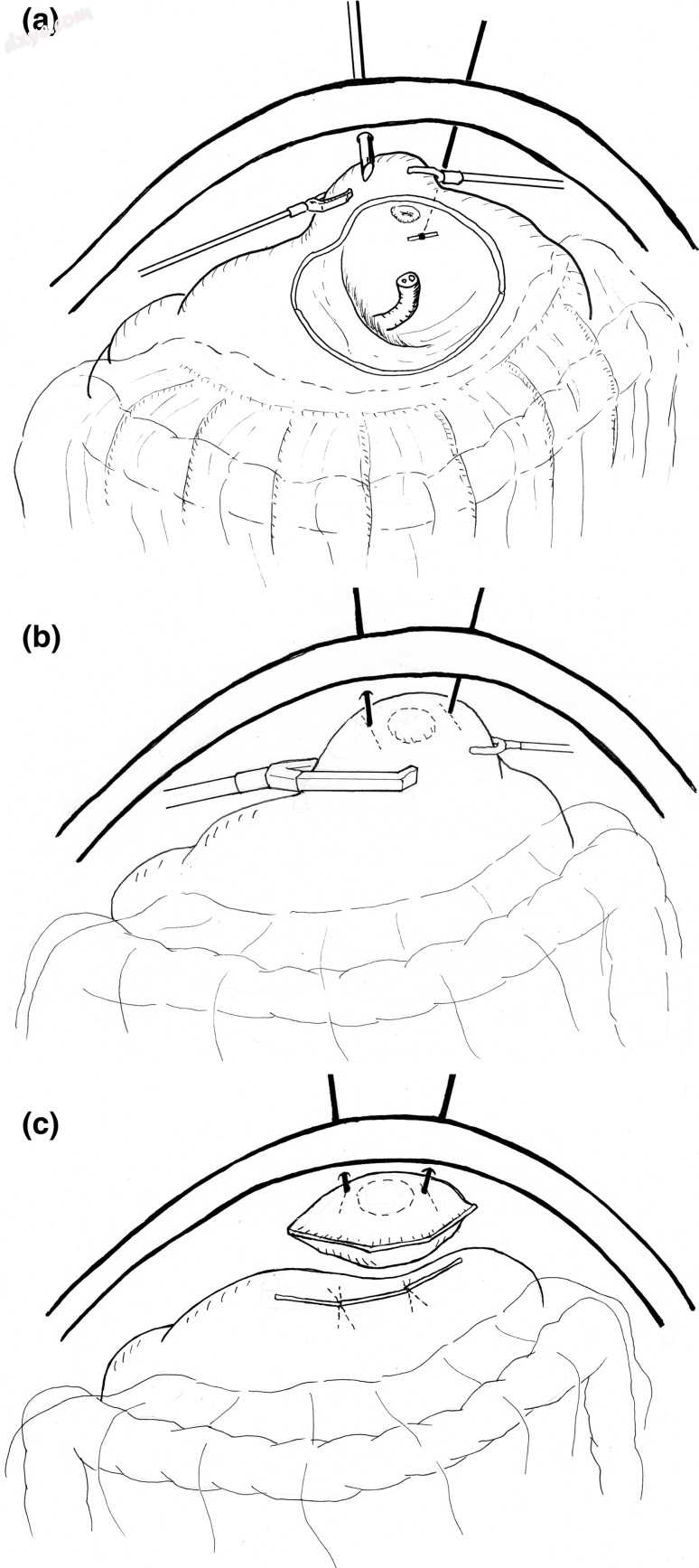
图1
腹腔镜局部切除术的病变提升方法。 a当患者处于仰卧位时,在胃镜引导下,在胃壁提升装置的T形杆上进行胃穿刺,经腹腔穿刺。 b然后用两个T形杆抬起病变,并且线性吻合器的多次激发有助于整块切除病变。整个过程在胃镜视觉下进行,以确保病变不包括在缝合缝合线中。 c使用线性吻合器同时进行切除和缝合后,收集样本并将其取出到样本收集袋中
非触摸病变提升[16]是腹腔镜局部切除胃的另一种方法(图2)。这是切除​​形成硬块的粘膜下肿瘤(例如GIST)的极好方法。然而,在浆膜和粘膜之间发生剪切的可能性使得难以实现粘膜病变的精确切除。该技术可能潜在地导致粘膜或胃壁的必要切除,并因此在切除大的病变时引起胃变形。
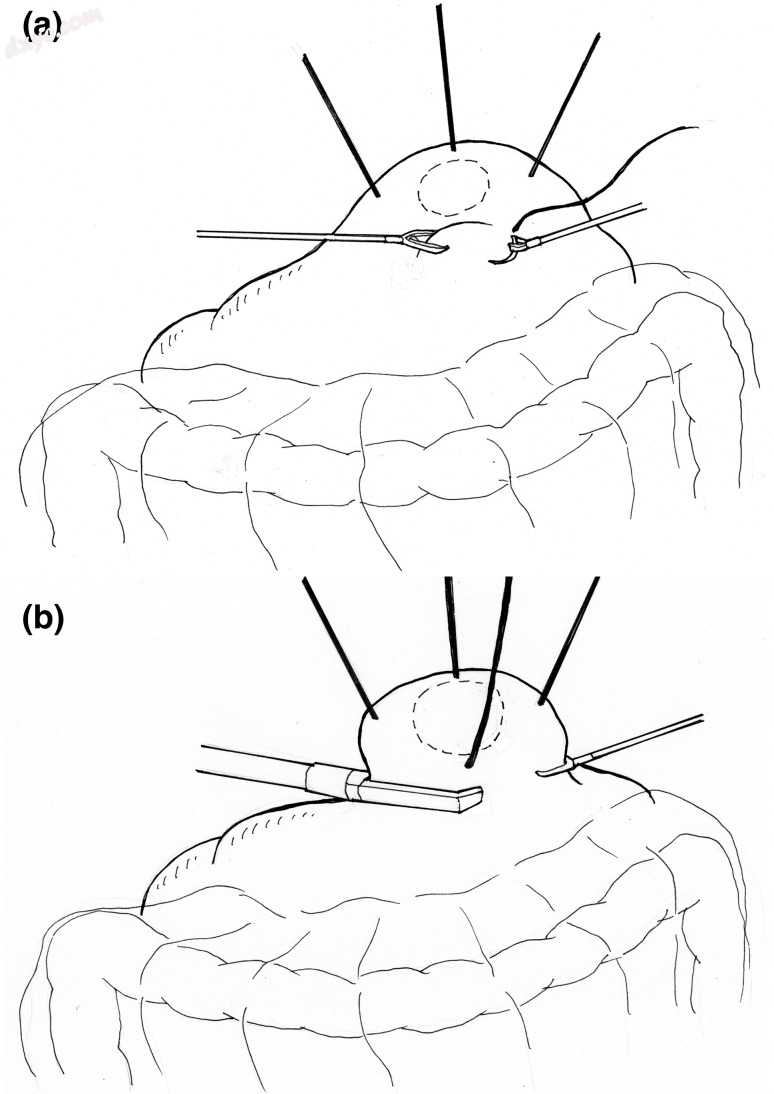
图2
腹腔镜局部切除术的非触摸病变提升方法。 a腹腔镜下放置的牵引缝合线位于肿瘤周围的健康浆膜中,取代了T形棒所起的作用。 b使用这些缝合线抬起病灶,通过线性吻合器的多次点火实现整块切除
使用柔性胃镜局部切除胃
内窥镜全层切除术(EFTR)是腹腔镜检查的另一种选择,其中胃镜用于腔内入路以实现胃的全层切除[17,19]。
胃壁穿孔是与EMR相关的并发症[13],当胃壁的整个厚度被错误地固定而不是在套管期间固定粘膜下层时,可以遵循无意的全厚度切除。这是一种严重的并发症,但如果可以用内窥镜放置的夹子封闭穿孔,则可以在不进行进一步手术的情况下进行治疗。 ESD的穿孔频率高于EMR,但关闭穿孔的技术不断改进,单纯穿孔很少需要外科手术[18]。 EFTR是指一种利用胃镜进行计划的全厚度胃切除术的技术,并且基于内窥镜闭合胃穿孔所描述的技术,通过内窥镜将其闭合。由EFTR管理的主要病变是小的粘膜下肿瘤。
目前,报告描述了具有小腔内生长的GIST的EFTR [20-23]。具有这种损伤的EFTR的重要性在于,在手术过程中损失的胃壁的范围很小,因此可以避免腹腔镜手术。与EFTR相关的缺点是适合切除的肿瘤尺寸有限,难以准确设计切除范围,内窥镜胃壁闭合困难,往往需要最终腹腔镜缝合,出血偶尔可能具有挑战性,并且潜在风险对其他器官造成伤害。由于这些原因,EFTR仍应被视为一种调查疗法。然而,随着最近推出的超范围夹(OTSC),这是一种特殊的胃穿孔闭合装置,它比以前更容易关闭胃壁缺损[24]。 EFTR有可能进行技术改进,因此预计其使用适应症将在未来扩展到小GIST的切除范围之外。
使用腹腔镜和胃镜进行胃的局部切除
如前所述,很难通过腹腔镜局部切除胃来确定最佳切除线,其结果是潜在的主要胃壁切除导致变形或排空受损。 另一方面,EFTR可以进行最小的切除,但是它存在胃壁缝线闭合以及尺寸和部位限制的问题。 产生的问题是,是否可以通过同时切除胃镜切开粘膜,腹腔镜切开浆膜层来克服这些限制,从而能够在几乎没有变形的情况下进行安全切除。 已经开发了这样的技术并且统称为腹腔镜内窥镜协同手术(LECS)(图3)。
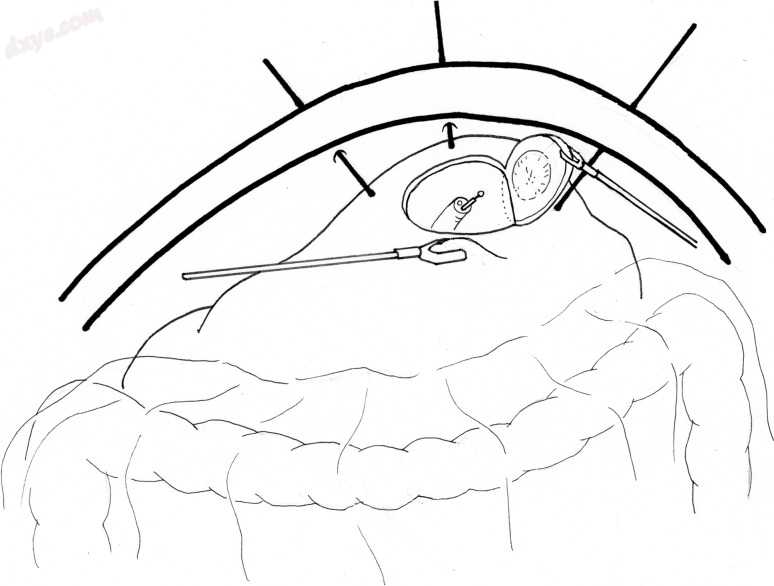
图3
腹腔镜内镜下联合手术治疗局部切除术。该图显示了小癌症的冠法。牵引缝合线腹腔镜放置在肿瘤周围的健康浆膜中。在这些缝线牵引病灶的情况下,内窥镜医师使用ESD装置进行全厚度切除。使用胃镜在腔内移除病灶后,使用腹腔镜通过手工缝合来关闭胃壁的缺损
使用腹腔镜和胃内窥镜进行胃部局部切除的概念并不新鲜,并且腹腔镜 - 内窥镜协作已经与病变提升技术一起实施。 LECS的新颖之处在于,首先使用ESD的粘膜切口技术来确定粘膜侧的切除线。 LECS最初是由Hiki等人开发的。 [25]作为腹腔镜局部切除胃的改进,用于5厘米及更小的GIST。首先,内窥镜医师在ESD中进行全周粘膜切口。然后,外科医生在超声波激活装置的帮助下腹腔镜切开浆膜层。该切口加深以包括胃壁的剩余厚度。在完全切除之前,将肿瘤转移到浆膜方面。通过在其上发射线性吻合器来同时完成切除,从而实现最终切除。收集肿瘤并在标本收集袋中取出。目前,LECS被用作涉及ESD和腹腔镜相结合的手术的一般术语,用于涉及胃肠道的手术[26]。与EFTR不同,LECS广泛且常规地执行,并且随着一些报告各种改进的研究人员不断发展。对于经典的LECS,胃腔通向腹腔,偶尔会有胃内容物溢出到腹膜腔中。然而,在胃癌的情况下,腹膜内溢出与肿瘤传播的风险相关。因此,将LECS应用于早期胃癌将需要一种方法来防止胃内容物的腹膜内溢出。报道的防止溢出的方法,包括倒置LECS(Crown方法)[27],CLEAN-NET [28]和NEWS [29],既有优点也有局限性,到目前为止还没有人能够获得广泛的普及。
胃癌局部切除的挑战和未来前景
如上所述,ESD的出现及其日益普及可能已经结束了胃局部切除早期胃癌的作用。然而,必须讨论这是否已经将胃的局部切除作为过去的操作降级。
有关适应症的挑战和未来前景
目前,在日本,虽然大部分分化的粘膜癌通过ESD切除,但手术仍用于粘膜下癌症和低分化腺癌。在大多数这些病例中,手术涉及腹腔镜胃切除术[30],淋巴结清扫达到'D1 +'。在这些手术切除病例中,只有20%有淋巴结转移。这意味着近80%的此类病例经历了不必要的淋巴结清扫,因此胃切除术的范围过大。更好的术前准确识别淋巴结转移的存在与否的技术将增加早期胃癌病例的比例,避免不必要的解剖,并恢复局部切除胃的重要性。
然而,除了常规的临床病理分析之外,没有方法可以识别术前淋巴结转移阴性的病例。因此,基于图像的胃癌淋巴结转移诊断仍然不足。这是因为早期胃癌中的大多数淋巴结转移是微观的,即使在非常小的淋巴结中也可以观察到它们[31]。目前诊断淋巴结转移最准确的方法是通过前哨淋巴结(SLN)活检进行术中诊断。前哨淋巴结是淋巴结,是第一个接受癌症病灶淋巴流的淋巴结[32]。 Sentinel节点概念表明癌症淋巴结转移的第一个迹象是哨点的微转移,这意味着在前哨淋巴结中没有转移的情况下淋巴结转移呈负面状态。 SLN概念对早期胃癌的有效性已被广泛讨论[33-37],最近的多中心前瞻性研究证明SLN理论是正确的[38]。 SLN活检的灵敏度为93%,准确度为99%,这表明SLN活检是决定是否进行淋巴结清扫之前需要考虑的可靠指标。
然而,虽然早期胃癌中SLN活检的有效性已经确定,但其诊断准确性存在相当大的差异。 SLN活组织检查需要多个部门之间的合作,技术上很困难,并且学习曲线陡峭,因此使其成为一种先进的诊断技术。使用SLN活检作为具有淋巴结阴性状态的早期胃癌的指标以应用胃的局部切除将需要SLN活组织检查技术的进一步创新以克服技术熟练的需要。这种突破预计来自荧光引导的SLN活组织检查[39,40]和新示踪剂的开发[41]。
有关切除手术的挑战和未来前景
虽然SLN活检可以确定适当的病例,但早期胃癌的局部切除面临着与GIST不同的技术障碍。
首先,由于难以对组织学上的胃癌侵袭性进行准确的术前诊断,因此确保负边缘也是困难的。在某些早期胃癌病例中,如果癌症发生在严重萎缩性胃炎的背景下,很难确定浸润程度[42]。此外,由于非连续隐窝进展的共存,低分化腺癌可能表现出比预期更大的传播,这在内窥镜检查中并不明显[43]。与GIST相比,治疗性切除的边缘较小,胃癌的根治性切除需要对术前的准确评估,以确保维持建议的边缘。但是,如果边缘太宽,那么局部切除的好处就会丧失。
第二个障碍涉及防止胃内容物腹膜内溢出到腹膜中。有报道称早期胃癌并发ESD期间穿孔引起腹膜转移复发[44]。腹膜转移的发生可能与伴随胃穿孔的肿瘤溢出有关。因此,在胃癌的局部切除术中,有必要防止胃内容物的腹膜内溢出并使肿瘤暴露最小化[26]。虽然这可以通过病变解除来实现,但使用EFTR和LECS可能很难做到这一点。已经开发了各种用于防止胃内容物溢入腹腔并完成LECS的技术[26-29]。已经报道了一种称为密封LECS的方法,其中在进行LECS之前将切除部位与浆膜表面密封[45]。然而,由于操作器械的自由度和视角受到限制,腹腔镜手术目前在开发这种技术方面具有局限性。机器人手术[46]可以为这些困难提供理想的解决方案。
局部切除胃的意义的挑战和未来前景
选择局部切除早期胃癌的原因是为了保持胃容量并最大限度地减少功能障碍,但与更彻底的手术相比,局部切除胃部在术后主诉或功能优势方面的真正好处尚不清楚。有关少数患者的研究报告了有利的结果。然而,应该注意的是,偶尔患者会因胃排空延迟而出现严重的术后症状[47]。众所周知,淋巴结清扫会对胃动力产生不利影响,导致幽门或胃的迷走神经去神经支配。 Kinami在调查需要随后进行矫正手术的有限手术病例后,观察到局部切除后避免功能障碍需要确保充足的血液流向胃残余并防止切除期间的变形[47]。
继续保存大部分胃的缺点也不容忽视。首先是胃残留中发生癌症的风险升高。异位多发性胃癌经常发生在远端部分胃切除术后的残余[48]和ESD [49]。因此,在对胃癌进行局部切除的情况下,其频率可能高于远端部分胃切除术后胃残留中的癌症发病率。要考虑的最重要的行动是早期发现异时性多发性胃癌。在适合ESD的阶段定期进行内镜下随访以发现胃残余癌,既不会对预后产生不利影响,也不会导致胃容量减少。要解决的问题是确定内窥镜随访的适当间隔。下一个重要行动是预防。鉴定胃残余癌症复发风险高的病例可能会考虑将其用于常规手术或制定严格的随访方案。高风险病例包括患有同步多发性胃癌的患者,ESD后的异时性多发性胃癌以及有胃癌家族史的患者。将来,使用分子生物学技术进行分析可以筛查出患多种胃癌风险的病例。另一项预防措施是根除幽门螺杆菌,目前正在进行静脉注射[50]。
胃部局部切除胃癌:一种理想的模型
Takagi等。 [51]报道了一种局部切除联合手术与EMR治疗早期胃癌的方法(图4),在腹腔镜手术时代之前。该方法令人惊讶地类似于“结合前哨淋巴结活检以确认患者转移阴性,通过LECS或EFTR进行胃部局部切除,并通过手术缝合修复它”的方法(图5),这是目前最先进的调查治疗方法。 Takagi等人的方法。然后没有普及,但由于前哨淋巴结活检的技术发展和内窥镜手术设备的最新进展,它很可能在25年后复活。

图4
Takagi博士报道了早期胃癌局部切除的旧技术。 a手术前,在肿瘤周围的四个点进行和靶向活组织检查,以确保达到安全边界,然后通过EMR切除主要病变的中心以确定入侵深度。 如果活检结果显示粘膜癌,则进行剖腹手术。 b局部切除胃是通过设置在纹身部位之外的解剖线进行的。 还进行了由印度墨水染色的胃周节点的取样解剖,以评估淋巴结状态和分期

图5
胃局部切除胃的理想模型。 a在手术期间进行腹腔镜荧光引导的前哨淋巴结活检以验证淋巴结阴性状态。淋巴盆的整块解剖是通过腹腔镜进行的,并且明亮的节点被送到病理切片以进行术中微转移的分子诊断。 b使用ESD装置进行内窥镜全层胃切除术和使用腹腔镜或手术机器人进行手缝合闭合,以实现肿瘤学安全和保存良好的功能
然而,除了适应症之外,与胃癌局部切除相关的问题迄今尚未被视为至关重要。胃变形,功能障碍和多种胃癌的问题尚待解决。腹腔镜切除术是可变的,并且尚未被证实优于常规手术。鉴于这些问题,因此存在将胃局部切除作为研究治疗的趋势,仅在精心选择的病例中应用。
参考:
Local resection of the stomach for gastric cancer
1. Edge SB, Byrd DR, Compton CC, Fritz AG, Greene FL, Trotti A, editors. AJCC cancer staging manual, 7th edn. New York, Springer; 2010. p. 3–14.
2. Songun I, Putter H, Kranenbarg EM, Sasako M, van de Velde CJ. Surgical treatment of gastric cancer: 15-year follow-up results of the randomised nationwide Dutch D1D2 trial. Lancet Oncol. 2010;11:439–449. doi: 10.1016/S1470-2045(10)70070-X. [PubMed] [CrossRef] [Google Scholar]
3. Degiuli M, Sasako M, Ponti A, Vendrame A, Tomatis M, Mazza C, et al. Randomized clinical trial comparing survival after D1 or D2 gastrectomy for gastric cancer. Br J Surg. 2014;101:23–31. doi: 10.1002/bjs.9345. [PubMed] [CrossRef] [Google Scholar]
4. Nakada K, Ikeda M, Takahashi M, Kinami S, Yoshida M, Uenosono Y, et al. Characteristics and clinical relevance of postgastrectomy syndrome assessment scale (PGSAS)-45: newly developed integrated questionnaires for assessment of living status and quality of life in postgastrectomy patients. Gastric Cancer. 2015;18:147–158. doi: 10.1007/s10120-014-0344-4. [PubMed] [CrossRef] [Google Scholar]
5. Japanese Gastric Cancer Association Japanese gastric cancer treatment guidelines 2010 (ver. 3) Gastric Cancer. 2011;14:113–123. doi: 10.1007/s10120-011-0042-4. [PubMed] [CrossRef] [Google Scholar]
6. Fujita J, Takahashi M, Urushihara T, Tanabe K, Kodera Y, Yumiba T, et al. Assessment of postoperative quality of life following pylorus-preserving gastrectomy and Billroth-I distal gastrectomy in gastric cancer patients: results of the nationwide postgastrectomy syndrome assessment study. Gastric Cancer. 2016;19:302–311. doi: 10.1007/s10120-015-0460-9. [PubMed] [CrossRef] [Google Scholar]
7. Takiguchi N, Takahashi M, Ikeda M, Inagawa S, Ueda S, Nobuoka T, et al. Long-term quality-of-life comparison of total gastrectomy and proximal gastrectomy by Postgastrectomy Syndrome Assessment Scale (PGSAS-45): a nationwide multi-institutional study. Gastric Cancer. 2015;18:407–416. doi: 10.1007/s10120-014-0377-8. [PubMed] [CrossRef] [Google Scholar]
8. Kitaoka H, Yoshikawa K, Suzuki M, Yoshida S, Yamagushi H, Hirota T, et al. Study on local resection of the tumor with preservation of the regional lymph-nodes for early gastric cancer (in Japanese) Nihon Gan Chiryo Gakkai Shi. 1983;18:969–978. [PubMed] [Google Scholar]
9. Ohara T, Jyoshima Y, Sadatsuki E, Kondo Y. Possibility of limited surgery for early gastric cancer (in Japanese) Shokakigeka. 1985;8:15–19. [Google Scholar]
10. Iwanaga T, Koyama H, Imaoka M, Furukawa H, Hiratsuka M. Surgical outcome and prospective for early gastric cancer (in Japanese) Pharma Med. 1989;7:27–33. [Google Scholar]
11. Ohgami M, Otani Y, Kumai K, Kubota T, Kim YI, Kitajima M. Curative laparoscopic surgery for early gastric cancer: five years experience. World J Surg. 1999;23:187–192. doi: 10.1007/PL00013167. [PubMed] [CrossRef] [Google Scholar]
12. Tada M, Karita M, Yanai H, Takemoto T. Endoscopic therapy of early gastric cancer by strip biopsy (in Japanese with English abstract) Gan To Kagaku Ryoho. 1988;15:1460–1465. [PubMed] [Google Scholar]
13. Gotoda T. Endoscopic resection of early gastric cancer. Gastric Cancer. 2007;10:1–11. doi: 10.1007/s10120-006-0408-1. [PubMed] [CrossRef] [Google Scholar]
14. Gotoda T, Yanagisawa A, Sasako M, Ono H, Nakanishi Y, Shimoda T, et al. Incidence of lymph node metastasis from early gastric cancer: estimation with a large number of cases at two large centers. Gastric Cancer. 2000;3:219–225. doi: 10.1007/PL00011720. [PubMed] [CrossRef] [Google Scholar]
15. Oda I, Saito D, Tada M, Iishi H, Tanabe S, Oyama T, et al. A multicenter retrospective study of endoscopic resection for early gastric cancer. Gastric Cancer. 2006;9:262–270. doi: 10.1007/s10120-006-0389-0. [PubMed] [CrossRef] [Google Scholar]
16. Kiyozaki H, Saito M, Chiba H, Takata O, Rikiyama T. Laparoscopic wedge resection of the stomach for gastrointestinal stromal tumor (GIST): non-touch lesion lifting method. Gastric Cancer. 2014;17:337–340. doi: 10.1007/s10120-013-0272-8. [PubMed] [CrossRef] [Google Scholar]
17. Suzuki H, Ikeda K. Endoscopic mucosal resection and full thickness resection with complete defect closure for early gastrointestinal malignancies. Endoscopy. 2001;33:437–439. doi: 10.1055/s-2001-14269. [PubMed] [CrossRef] [Google Scholar]
18. Fujishiro M, Yahagi N, Kakushima N, Kodashima S, Muraki Y, Ono S, et al. Successful nonsurgical management of perforation complicating endoscopic submucosal dissection of gastrointestinal epithelial neoplasms. Endoscopy. 2006;38:1001–1006. doi: 10.1055/s-2006-944775. [PubMed] [CrossRef] [Google Scholar]
19. Ikeda K, Mosse CA, Park PO, Fritscher-Ravens A, Bergström M, Mills T, et al. Endoscopic full-thickness resection: circumferential cutting method. Gastrointest Endosc. 2006;64:82–89. doi: 10.1016/j.gie.2005.12.039. [PubMed] [CrossRef] [Google Scholar]
20. Zhou PH, Yao LQ, Qin XY, Cai MY, Xu MD, Zhong YS, et al. Endoscopic full-thickness resection without laparoscopic assistance for gastric submucosal tumors originated from the muscularis propria. Surg Endosc. 2011;25:2926–2931. doi: 10.1007/s00464-011-1644-y. [PubMed] [CrossRef] [Google Scholar]
21. Shi Q, Chen T, Zhong YS, Zhou PH, Ren Z, Xu MD, et al. Complete closure of large gastric defects after endoscopic full-thickness resection, using endoloop and metallic clip interrupted suture. Endoscopy. 2013;45:329–334. doi: 10.1055/s-0032-1326214. [PubMed] [CrossRef] [Google Scholar]
22. Ye LP, Yu Z, Mao XL, Zhu LH, Zhou XB. Endoscopic full-thickness resection with defect closure using clips and an endoloop for gastric subepithelial tumors arising from the muscularis propria. Surg Endosc. 2014;28:1978–1983. doi: 10.1007/s00464-014-3421-1. [PubMed] [CrossRef] [Google Scholar]
23. Yang F, Wang S, Sun S, Liu X, Ge N, Wang G, et al. Factors associated with endoscopic full-thickness resection of gastric submucosal tumors. Surg Endosc. 2015;29:3588–3593. doi: 10.1007/s00464-015-4113-1. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
24. Guo J, Liu Z, Sun S, Liu X, Wang S, Ge N, et al. Endoscopic full-thickness resection with defect closure using an over-the-scope clip for gastric subepithelial tumors originating from the muscularis propria. Surg Endosc. 2015;29:3356–3362. doi: 10.1007/s00464-015-4076-2. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
25. Hiki N, Yamamoto Y, Fukunaga T, Yamaguchi T, Nunobe S, Tokunaga M, et al. Laparoscopic and endoscopic cooperative surgery for gastrointestinal stromal tumor dissection. Surg Endosc. 2008;22:1729–1735. doi: 10.1007/s00464-007-9696-8. [PubMed] [CrossRef] [Google Scholar]
26. Hiki N, Nunobe S, Matsuda T, Hirasawa T, Yamamoto Y, Yamaguchi T. Laparoscopic endoscopic cooperative surgery. Dig Endosc. 2015;27:197–204. doi: 10.1111/den.12404. [PubMed] [CrossRef] [Google Scholar]
27. Nunobe S, Hiki N, Gotoda T, Murao T, Haruma K, Matsumoto H, et al. Successful application of laparoscopic and endoscopic cooperative surgery (LECS) for a lateral-spreading mucosal gastric cancer. Gastric Cancer. 2012;15:338–342. doi: 10.1007/s10120-012-0146-5. [PubMed] [CrossRef] [Google Scholar]
28. Inoue H, Ikeda H, Hosoya T, Yoshida A, Onimaru M, Suzuki M, et al. Endoscopic mucosal resection, endoscopic submucosal dissection, and beyond: full-layer resection for gastric cancer with nonexposure technique (CLEAN-NET) Surg Oncol Clin N Am. 2012;21:129–140. doi: 10.1016/j.soc.2011.09.012. [PubMed] [CrossRef] [Google Scholar]
29. Goto O, Mitsui T, Fujishiro M, Wada I, Shimizu N, Seto Y, et al. New method of endoscopic full-thickness resection: a pilot study of non-exposed endoscopic wall-inversion surgery in an ex vivo porcine model. Gastric Cancer. 2011;14:183–187. doi: 10.1007/s10120-011-0014-8. [PubMed] [CrossRef] [Google Scholar]
30. Yamashita K, Sakuramoto S, Kikuchi S, Futawatari N, Kataba N, Hosoda K, et al. Laparoscopic versus open distal gastrectomy for early gastric cancer in Japan: long-term clinical outcomes of a randomized clinical trial. Surg Today. 2016;46:741–749. doi: 10.1007/s00595-015-1221-4. [PubMed] [CrossRef] [Google Scholar]
31. Noda N, Sasako M, Yamaguchi N, Nakanishi Y. Ignoring small lymph nodes can be a major cause of staging error in gastric cancer. Br J Surg. 1998;85:831–834. doi: 10.1046/j.1365-2168.1998.00691.x. [PubMed] [CrossRef] [Google Scholar]
32. Morton DL, Wen DR, Wong JH, Economou JS, Cagle LA, Storm FK, et al. Technical details of intraoperative lymphatic mapping for early stage melanoma. Arch Surg. 1992;127:392–399. doi: 10.1001/archsurg.1992.01420040034005. [PubMed] [CrossRef] [Google Scholar]
33. Miwa K. Sentinel node concept and its application for cancer surgery (in Japanese with English abstract) Nihon Geka Gakkai Zasshi. 2000;101:307–310. [PubMed] [Google Scholar]
34. Hiratsuka M, Miyashiro I, Ishikawa O, Furukawa H, Motomura K, Ohigashi H, et al. Application of sentinel node biopsy to gastric cancer surgery. Surgery. 2001;129:335–340. doi: 10.1067/msy.2001.111699. [PubMed] [CrossRef] [Google Scholar]
35. Carlini M, Carboni F, Petric M, Santoro R, Guadagni F, Marandino F, et al. Sentinel node in gastric cancer surgery. J Exp Clin Cancer Res. 2002;21:469–473. [PubMed] [Google Scholar]
36. Ichikura T, Morita D, Uchida T, Okura E, Majima T, Ogawa T, et al. Sentinel node concept in gastric carcinoma. World J Surg. 2002;26:318–322. doi: 10.1007/s00268-001-0226-x. [PubMed] [CrossRef] [Google Scholar]
37. Kitagawa Y, Fujii H, Mukai M, Kubota T, Otani Y, Kitajima M. Radio-guided sentinel node detection for gastric cancer. Br J Surg. 2002;89:604–608. doi: 10.1046/j.1365-2168.2002.02065.x. [PubMed] [CrossRef] [Google Scholar]
38. Kitagawa Y, Takeuchi H, Takagi Y, Natsugoe S, Terashima M, Murakami N, et al. Sentinel node mapping for gastric cancer: a prospective multicenter trial in Japan. J Clin Oncol. 2013;31:3704–3710. doi: 10.1200/JCO.2013.50.3789. [PubMed] [CrossRef] [Google Scholar]
39. Kinami S, Oonishi T, Tomita Y, Kaida D, Funaki H, Fujita J, et al. Optimal setting and accuracy of indocyanine green fluorescence imaging for sentinel node biopsy in early gastric cancer. Oncol Lett. 2015. (in press). [PMC free article] [PubMed]
40. Fujimura T, Fushida S, Tsukada T, Kinoshita J, Oyama K, Miyashita T, et al. A new stage of sentinel node navigation surgery in early gastric cancer. Gastric Cancer. 2015;18:210–217. doi: 10.1007/s10120-014-0446-z. [PubMed] [CrossRef] [Google Scholar]
41. Brouwer OR, Buckle T, Vermeeren L, Klop WM, Balm AJ, van der Poel HG, et al. Comparing the hybrid fluorescent-radioactive tracer indocyanine green-99mTc-nanocolloid with 99mTc-nanocolloid for sentinel node identification: a validation study using lymphoscintigraphy and SPECT/CT. J Nucl Med. 2012;53:1034–1040. doi: 10.2967/jnumed.112.103127. [PubMed] [CrossRef] [Google Scholar]
42. Mishima T, Hamamoto H, Miyake N, Okuzono T, Mizuno H, Miyashita Y, et al. Endoscopic diagnosis of the intramucosal extent of infiltration in flat-type, early gastric cancers (in Japanese with English abstract) Stomach Intestine. 2010;45:39–48. [Google Scholar]
43. Yagi K, Satou T, Nakamura A, Sekine A. The possibility and limitation of magnifying endoscopic diagnosis using NBI in the extent of undifferentiated intramucosal gastric adenocarcinoma (in Japanese with English abstract) Stomach Intestine. 2009;44:60–70. [Google Scholar]
44. Morita A, Yabushita K, Kimura J, Oyama K, Terada I, Yamamoto S, et al. A case of stage IB gastric cancer caused peritoneal dissemination in 1 year after perforation during endoscopic submucosal dissection (in Japanese with English abstract) Jpn J Gastroenterol Surg. 2007;40:399–404. doi: 10.5833/jjgs.40.399. [CrossRef] [Google Scholar]
45. Kitakata S, Itoh T, Kinami S, Kawaura K, Hamada K, Kosaka T. Sentinel node navigated sealed EFTR for early gastric cancer (in Japanese) Operation. 2015;69:1465–1471. [Google Scholar]
46. Obama K, Sakai Y. Current status of robotic gastrectomy for gastric cancer. Surg Today. 2016;46:528–534. doi: 10.1007/s00595-015-1190-7. [PubMed] [CrossRef] [Google Scholar]
47. Kinami S, Fujimura T, Fushida S, Miyashita T, Ninomiya I, Fujita H, et al. The pitfalls and measures for pylorus preserving procedure in the limited surgery for early gastric cancer (in Japanese) Surg Therapy. 2007;96:1067–1074. [Google Scholar]
48. Hosokawa O, Kaizaki Y, Morishita M, Hattori M, Douden K, Hayashi Y, et al. Prolonged endoscopic surveillance of gastric remnant cancer after early cancer surgery (in Japanese with English abstract) Stomach Intestine. 2004;39:985–995. [Google Scholar]
49. Kobayashi M, Narisawa R, Sato Y, Takeuchi M, Aoyagi Y. Self-limiting risk of metachronous gastric cancers after endoscopic resection. Digest Endosc. 2010;22:169–173. doi: 10.1111/j.1443-1661.2010.00987.x. [PubMed] [CrossRef] [Google Scholar]
50. Yoon SB, Park JM, Lim CH, Cho YK, Choi MG. Effect of Helicobacter pylori eradication on metachronous gastric cancer after endoscopic resection of gastric tumors a meta-analysis. Helicobacter. 2014;19:243–248. doi: 10.1111/hel.12146. [PubMed] [CrossRef] [Google Scholar]
51. Takagi K, Iwakiri K, Takenaga S, Hayashi S. Local resection of the stomach applied with endoscopic resection for early gastric cancer—a point of contact between endoscopic treatment and limited surgery—(in Japanese with English abstract) Jpn J Gastroenterol Surg. 1993;26:2542–2547. doi: 10.5833/jjgs.26.2542. [CrossRef] [Google Scholar] |


