马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?注册
×
概要
穿支皮瓣的引入代表了显微外科重建的重大进步。然而,由于错误地认为穿支皮瓣不同于传统的皮瓣,因此出现了混乱。穿支的概念并不新鲜,但是从传统的皮瓣演变而来。事实上,显微镜使用的一些皮瓣是穿支皮瓣。唯一的区别是所涉及的血管的解剖水平;穿支的概念主要集中在远端循环,即所谓的“射孔器”。因此,可以从肌皮瓣的常规供体部位取出较薄的组织切片。通过使用穿支,不再需要用于特定重建的“选择瓣”,因为常规供体部位已成为通用供体部位,从而能够收获各种皮瓣。此外,根据外科医生的能力,任何皮瓣都可以用作基于穿支的岛状皮瓣,其源血管已完全保存。因此,可以有效地定制组织并将其定制为重建所需的任何配置。穿支皮瓣技术的应用可以实现更精确的解剖,并允许更有选择性地收获更薄的皮瓣,这将扩大重建手术的选择范围。毫无疑问,这项技术将继续发展。
图形摘要
关键词:外科皮瓣,穿支皮瓣,显微外科,重建
介绍
与使用传统皮瓣相比,穿支皮瓣在重建手术中的使用是一种优越的手术技术。最初,基于穿孔容器或“穿支”的皮瓣的概念被认为是新的并且不同于传统皮瓣(1,2)的旧概念。然而,穿孔技术实际上直接从传统方法演变而来,并且与传统方法没有很大不同。外科医生缺乏穿支皮瓣手术技术的经验,以及对该技术性质的困惑,导致误解穿支皮瓣手术难以进行。这种误解扩大到对支撑皮瓣和早期经典皮瓣之间区别的混淆。事实上,根据目前的定义,外科医生多年来使用的许多皮瓣实际上都是穿支皮瓣,尽管当时有许多不同的名称(1,2,3)。
穿支皮瓣技术的发展使人们更好地理解了皮瓣如何获得血液供应(3,4)。主要来源血管为它们穿过的所有组织提供营养血流。这些主要血管及其主要分支发送其他较小的分支来供应周围的肌肉,结缔组织和皮肤(5)。轴向图案皮瓣设计成在皮瓣基部包括轴向血管,以提供血液供应(2)。因此,重要的是要知道精确的血管解剖设计皮瓣,这是一个基于分支的概念。然而,随着皮瓣概念的发展,皮瓣设计从基于源船或分支概念演变为基于特定的射孔船。穿支皮瓣的成功收获需要识别穿孔血管,并以逆行方式(从远端到近端)解剖(6)。因此,进入蒂的路径发生了变化:在收获传统皮瓣时直接接近源血管是必不可少的,但是当采集穿支皮瓣时,该方法从皮下循环的远端部分开始组织层,并进入源血管。事实上,根据蒂(3,6,7)的解剖学变化,皮瓣收获通常是游离式的。射孔船的来源和路径不是操作的基本考虑因素,尽管穿支总是来自源血管(6)。有时,单独的穿支可以选择性地用作蒂(4),因此消除了近端解剖(3)。
在这里,作者回顾了皮瓣技术发展的历史方面,并提供穿支皮瓣的概述。穿支皮瓣技术的应用可以实现更精确的解剖,并允许更有选择性地收获更薄的皮瓣,这扩大了重建手术的选择范围。毫无疑问,这项技术将继续发展。
穿支皮瓣的概念和分类
总体而言,皮肤和皮下组织的脉管系统排列在五个血管丛中:表皮下神经丛,真皮丛,皮下神经丛,皮下神经丛和筋膜丛(筋膜下和上筋膜)。传统的肌皮瓣或筋膜皮瓣连接到肌肉下的源血管,或连接到筋膜水平的血管(5)。另一方面,穿支皮瓣连接到皮下或皮下神经丛的血管,因此与传统皮瓣(8,9)相比,其涉及更远端血管的连接。
根据穿支血管的路径,穿支可分为直接皮肤,皮下和肌皮穿支(10)。穿支的确切定义仍存在争议。当穿支的概念首次被引入时,Wei 等人。 (11)确定的射孔血管是源动脉深的那些射血管和直接将血液运送到筋膜皮肤组织的分支,在其到达皮肤的过程中,穿过悬垂的肌肉组织而不是仅仅跟随肌间隔。根据这个定义,只有肌皮穿支被认为是真正的穿支,而基于其他类型穿支的皮瓣不被视为穿支皮瓣。然而,这种严格的定义引起了穿支概念的混淆。前外侧大腿(ALT)皮瓣是最受欢迎的穿支皮瓣之一,是一个代表性的例子,它展示了穿支皮瓣和传统皮瓣之间的差异。前外侧皮瓣基于连接到外侧旋股骨系统的下行分支的穿支(6,12,13)。大多数情况下,穿支穿过股外侧肌(82%),因此是肌皮瓣,或者是一种皮瓣穿支,比肌皮穿支(14)更容易采集和使用。根据严格的定义,基于肌皮穿支的皮瓣是穿支皮瓣,基于皮瓣穿支的皮瓣不是穿支皮瓣。这些皮瓣在椎弓根夹层的容易性方面彼此不同 - 在肌皮瓣中进行繁琐的肌肉夹层,而不是在皮瓣皮瓣之间轻松快速地解剖(6,14)。大多数显微外科医生试图在穿支概念发展之前选择皮瓣穿支来节省手术时间,但是现在由于穿支的可靠性,肌肉夹层更受欢迎。此外,当穿支可靠且长度足够时,蒂夹层停止在穿支的水平,而不需要肌肉解剖(6)。因此,ALT皮瓣已从肌皮瓣演变为基于皮下或肌皮穿支的一系列皮瓣。由于重要的是要区分这些皮瓣,工作人员已经命名了不同的皮瓣'ALT肌皮瓣','侧旋股骨穿支皮瓣','股沟外侧穿支皮瓣'和'基于ALT穿支的皮瓣',取决于关于穿支(10)。前两种图案是传统的皮瓣,而后三种图案是穿支皮瓣。外侧旋支股动脉瓣可以包括在两组中:它最初被称为ALT(常规)皮瓣但现在被认为是穿支皮瓣,其说明围绕穿支概念的混淆。这就是作者坚持认为穿支皮瓣的概念与传统皮瓣概念完全不同的原因(图1)。因此,作者得出结论,先前描述为传统皮瓣的皮瓣实际上是穿支皮瓣,并且基于皮瓣穿孔的皮瓣应被视为穿支皮瓣(3,10)。
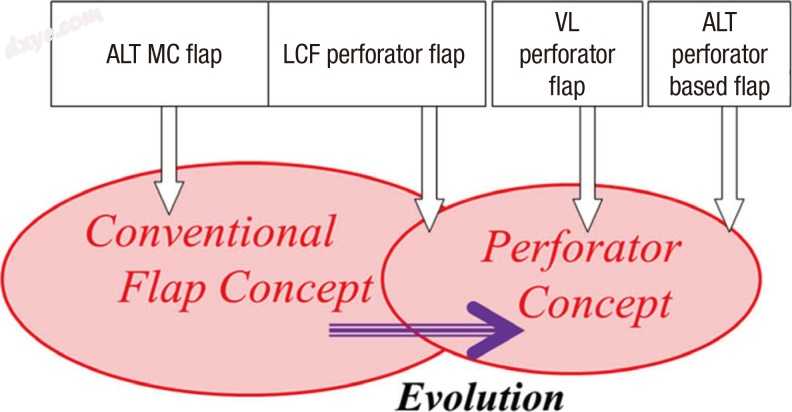
图. 1
传统皮瓣及其衍生的穿支皮瓣图。在引入穿支概念之前,ALP MC皮瓣和LCF穿支皮瓣(基于SCp)是常用的皮瓣。在引入穿支概念之后,LCF穿支皮瓣被认为是穿支皮瓣,并且挑战了VL穿支皮瓣(基于MCp)和基于ALT穿支的皮瓣。 LCF穿支皮瓣现在包含在这两个概念中,它是一个穿支皮瓣。因此,穿支不能完全区别于传统的皮瓣,并且一些经典的皮瓣实际上是穿支皮瓣,即使它们用不同的名称描述。 ALT MC皮瓣,股前外侧肌皮瓣; LCF穿支皮瓣,股外旋支穿支皮瓣; SCp,皮下穿支; VL穿支皮瓣,broadus lateralis穿支皮瓣; MCp,肌皮肤穿支。
现在大多数皮瓣基于其穿支而不是其源血管或分支而升高,并且穿支组中还应包括直接皮肤穿支(DCp)(3,10,15)。然而,就手术切除水平而言,所需的皮瓣穿支和DCP彼此之间并不十分不同,应与肌皮穿支器区分开来,这需要在升高时进行肌肉切除术(14)。因此,基于肌皮穿支的穿支皮瓣是以肌肉所涉及的名称命名的。另一方面,基于皮下穿支或直接皮肤穿支的皮瓣以其源血管命名(图2,图3)3)(10)。基于穿支本身的皮瓣,没有进一步的近端解剖,被称为穿支 - “基于”皮瓣并且以相关肌肉(MCp)或血管(SCp)命名(图4)(10,16)。
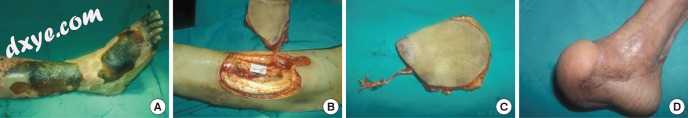
图2
股外侧肌穿支皮瓣。 (A)一名57岁的男性患者在右脚挤压伤后需要截肢时患有蜂窝织炎。 (B,C)基于肌皮穿支,提升12×15cm 股外侧肌穿支皮瓣。 (D)12个月随访时的术后观察。
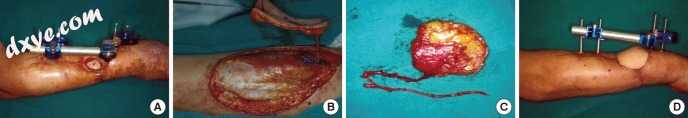
图3
侧旋回旋股骨穿支皮瓣。 (A)46岁患者的胫骨开放性骨折采用外固定器固定。 然而,随着胫骨的暴露,覆盖的皮肤变得坏死。 (B,C)10×8cm的外侧旋支股骨穿支皮瓣在流通模式中升高。 (D)皮瓣转移后两个月保持良好的轮廓。
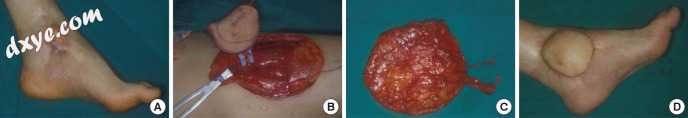
图4
基于股外侧肌穿支皮瓣。 (A)在内踝区域的不稳定烧伤瘢痕上存在复发性溃疡。 (B,C)清创后,以游离皮瓣为基础,将8×8 cm 股外侧肌穿支皮瓣抬高,并进行穿支 - 穿孔吻合术。 (D)术后3个月的观点。
历史意义
轴向皮瓣的概念是在20世纪70年代发展起来的。一项重大发现是由McGregor和Morgan(2)以及McGregor和Jackson(17)描述的椎弓根腹股沟皮瓣,基于结合的轴向血液供应。对皮瓣的血液供应的重要性限制了身体的特定区域中的皮瓣设计到轴向血液供应(2,5,18)。随后,更详细的血管解剖学知识允许更好的皮瓣选择和细化(图5)。由于在腹股沟区域存在多个穿支,皮瓣变得更加通用,并且自由式设计成为可能。因此,术语“腹股沟皮瓣”并不常用。取而代之的是,使用诸如“浅表髂髂穿支皮瓣”,“浅表下腹部穿支皮瓣”或“外阴部穿支皮瓣”之类的名称(图6,,7,7, 8)0.8)。在开发穿支概念之前,在教科书中描述了解剖腹股沟皮瓣收获的方法,并且提供了用于安全且成功的皮瓣收获的指南或标志。然而,随着穿支概念的发展,可以实现更多种类的皮瓣设计,并且可以更自由地修改采集的穿支皮瓣的尺寸和组成。例如,来自腹股沟区域的薄穿支皮瓣可用于四肢的薄表面重修;蒂皮瓣可用于生殖器表面重修;血管化淋巴结可以转移;可以采集体积更换的笨重皮瓣,例如用于乳房重建的笨重的浅表下腹壁穿支皮瓣(8,19)。通过穿支概念实现的更先进的外科技术允许常规供体部位成为“通用供体部位”,其根据患者的特定需要使得皮瓣的设计,组成和使用能够有更大的变化。穿支皮瓣不是一种新的,困难的皮瓣,而是将演化和改进的手术技术应用于更常见的传统皮瓣的产物。腹股沟带蒂皮瓣曾经是用于手部重铺的“选择皮瓣”,但现在腹股沟区域可以是各种穿支皮瓣的来源,这取决于所需要的。
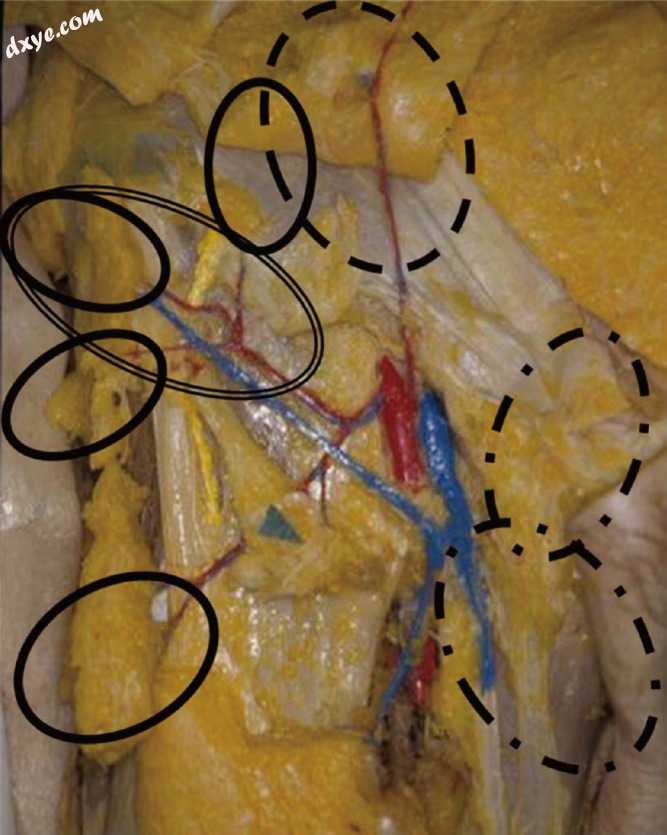
图5
腹股沟区域有腹股沟皮瓣和穿支皮瓣。 腹股沟皮瓣是以教科书式收获的传统皮瓣,常用于紧急手部表面。 在引入穿支概念后,几种不同的穿支皮瓣可用于各种重建目的; 例如,SIEp,SCIp,EPp皮瓣用于薄表面置换,血管化淋巴结转移或乳房重建。 设计和切口是自由式的,不考虑任何标志,并且皮瓣收获比传统的腹股沟皮瓣更简单和更快。 SIEp,浅表下腹壁穿支皮瓣; SCIp,浅表旋髂穿支皮瓣; EPP,外阴部穿支皮瓣。
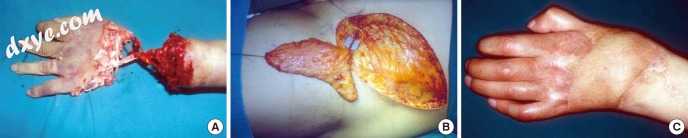
图6
薄薄的表面置换与浅表下腹壁穿支皮瓣。 (A)32岁患者,左手被截肢。 (B)再植后,手背需要薄的表面重修,并收获浅表下腹壁穿支皮瓣。 (C)重铺后的术后6个月视图。
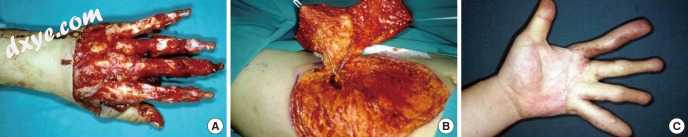
图7
薄薄的表面旋转髂骨穿支皮瓣表面重修。 (A)一名47岁的患者,他的所有手指都有脱臼伤害。 (B)收获15×22cm浅表旋髂穿支皮瓣用于表面重修,然后在3个月后分割皮瓣。 (C)患者能够用手指的自然轮廓夹住并抓住。
图8
使用外阴部穿支岛状皮瓣进行阴囊重建。 (A)一名29岁的患者因阴道睾丸而阴囊丢失。 (B)使用双侧外阴部穿支岛状皮瓣进行阴囊重建。 (C)重建后6个月,通过薄皮瓣重建获得阴囊的自然形状,并隐藏沿腹股沟褶皱的供体部位瘢痕。
结果表明,皮肤通过身体许多区域的下层肌肉获得血液供应(5)。这一发现导致了肌皮瓣的发展。这些皮瓣的成功使用可归因于肌肉的强大血液供应(14,20,21,22,23)。然而,收获肌肉经常导致随后的供体部位功能丧失,并且所产生的皮瓣的蓬松性经常导致不准确的重建和差的美学效果(1)。在同一时期,包括深筋膜,并依赖于筋膜水平(筋膜下和超筋膜丛)的血管,导致了非常可靠的筋膜皮瓣(14,24,25,26)的发展。 1989年,Koshima和Soeda(27)推出了一种基于穿支的新型皮瓣,它仅由皮肤和皮下组织组成。这种皮瓣与筋膜皮瓣不同。筋膜丛不是血管形成所必需的(3,27,28)。如果保留肌肉的小动脉并使皮肤血管化(肌肉穿孔),则可以排除肌肉(3,14,27)。穿支皮瓣的使用是对肌肉皮瓣的使用的改进,并且使得肌肉本身可以留下(1,14,19,27,29)。
皮瓣的演变
用薄皮瓣重新铺设
进行薄表面重修的能力是穿支皮瓣(3,9,13)的优点之一。通过提升仅包含表面脂肪层(10,16)的薄皮瓣,可以减小用于塑形或表面重修的皮瓣的厚度。皮下层由浅表和深脂肪层(30)组成。表面脂肪层具有恒定的厚度,更多的血管分布,并且由小的粉红色脂肪颗粒组成。另一方面,深脂肪层具有可变的厚度,较小的血管分布,并且由大的黄色脂肪颗粒组成。通过排除深部脂肪层(16),基于穿支的恒定厚度的皮瓣可以在很大的距离上升高。使用单极电烙术并且使皮瓣保持在皮肤钩的张力下,皮瓣可以在浅表和深脂肪层(16,31)之间变薄。
传统的捐助地点变得普遍
可以采集背阔肌肌皮瓣的侧胸区现在用作穿支皮瓣的供体部位,如背阔肌穿支(LDP)皮瓣,胸背穿支(TDp)皮瓣和侧胸廓穿支。 (LTp)皮瓣(图9)(16,31)。覆盖在胸外侧区域的皮肤来自三排穿支的血液供应丰富,这些穿支来自胸背和胸外侧血管(31,32)。从前到后,胸外侧区域的三组穿支是:1)来自胸外侧动脉的直接皮肤穿支,2)胸背动脉的皮肤穿支,3)来自胸背动脉的肌皮穿支(16, 31,32)。这些穿支具有与穿支皮瓣的椎弓根相同的可靠性。由于它们都可以被认为来自同一供体部位(31,32),因此必须通过不同的命名法来区分它们。根据作者的命名法,基于皮瓣穿支或直接皮肤穿支的皮瓣以近端血管命名,而基于肌皮穿支的皮瓣以肌肉命名(10,31)。因此,'背阔肌穿支皮瓣'表示基于肌皮穿支的穿支皮瓣,'胸背的穿支皮瓣'是基于皮肤穿支的穿支皮瓣,以及'侧胸穿支皮瓣'是基于胸外侧动脉的直接皮肤穿支(10,33)。因此,在穿支概念的背景下,肌肉或肌皮瓣的常规供体部位变成“通用供体部位”。
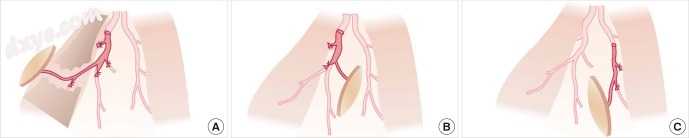
图9
三个穿支皮瓣从胸外侧区域。 (A)背阔肌穿支(LDp)皮瓣。 (B)胸背穿支(TDp)皮瓣。 (C)侧胸廓穿支(LTp)皮瓣。
没有更多“选择的皮瓣”
当计划在胸外侧区域的供体部位的主要闭合时,可以安全地设计长度为20cm,宽度为10cm的薄皮瓣(31)。这些护翼可以有效地用于手,前牙或脚(16)的表面重修。而且,它们可以很容易地成形和设计以适应缺陷。在舌头重建的情况下,皮瓣可以以薄的包裹图案成形为金字塔形,或者具有适中的厚度以形成舌根。此外,可以将较大的皮瓣定制成用于食管重建的管状皮瓣,这比使用腹部手术用于空肠皮瓣收获容易得多。在另一种情况下,穿支皮瓣可用于半侧重建(图10)。前臂和空肠皮瓣是头部,颈部和食管重建的“选择皮瓣”。现在,这些皮瓣正在被穿支皮瓣取代,因为后者在设计和组成方面更加多样化和多样化(12,15)。改进对血管解剖学的了解和理解,可以更好地定制皮瓣,并改进所涉及的重建手术(15,19)。
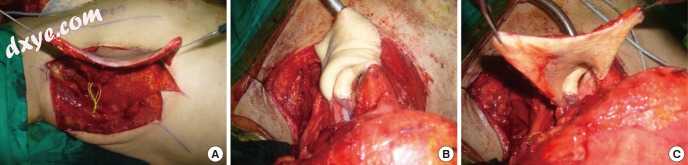
图10
半喉咽的重建。 (A)喉部穿支皮瓣抬高用于喉癌患者的半侧重建。 (B,C)将超薄侧胸外穿支皮瓣折叠并成形以产生真正的声带和假声带的曲率。
定制/量身定制的重建
改进的血液供应知识以及穿支概念的发展已经增加了外科医生可获得的皮瓣软组织成分的多样性(15,16)。 皮肤脂肪的皮瓣,脂肪皮瓣,脂肪筋膜的皮瓣和肌筋膜筋膜的皮瓣都可以从相同的供体部位收获,从而改善皮瓣的剪裁和更多的重建细化(13,33,34)。对于患有上颌癌的患者,皮瓣的每个穿支部件必须根据缺损的大小和组成进行调整,这需要重建口腔衬里,鼻内层和面颊的外部表面重修(35)。这种程度的定制或定制重建是可能的,因为穿支皮瓣可以具有适当的组成,允许它们像缺失块的组件一样插入缺陷中。对于具有上唇静脉畸形的另一患者,可以利用游离皮瓣在肿瘤消融后消除死腔并防止肿瘤复发。在根治性切除血管瘤后,将支撑皮瓣定制为类似于来自肿瘤的切除组织(图11)。
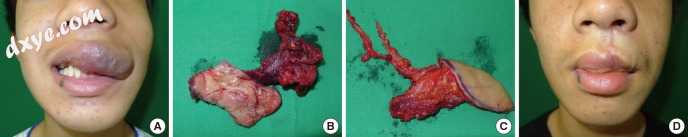
图11
定制重建上唇。 (A)一名14岁的男性在他的上唇和左脸颊上出现静脉畸形。 (B)彻底切除静脉畸形。 (C)一个5×3厘米,薄的侧胸穿支皮瓣设计用于上唇重建。 (D)手术后6个月,静脉畸形逐渐消退,没有复发。
基于穿支的岛状皮瓣
穿支皮瓣的一个潜在应用是使用与缺损相邻的组织作为基于穿支的岛状皮瓣(PBIF)。当皮瓣真正基于穿支本身时,术语“基于穿支”用于皮瓣,保存近端血管(10,16);解剖在上筋膜或肌内水平暂停,而不需要牺牲近端血管(31)。 PBIF可以从任何存在穿支的区域升高,为翼片(16,31,34,36,37)的设计提供更大的自由度。重建变得简单,在选择合适的设计时提供了更多选择,并解决了以前需要自由翻盖的问题(25,36,37)。例如,前臂皮瓣是筋膜皮瓣,其中包括隔膜和深筋膜,需要牺牲桡动脉和静脉。通过使用单个穿支,相关的皮瓣与类似尺寸的岛状皮瓣(15)相当。在导致跟腱暴露的小缺陷的情况下,常规治疗涉及侧跟骨瓣,其需要牺牲源血管以及供体部位处的皮肤移植物。然而,通过使用PBIF,可以保存源血管并且可以在不需要皮肤移植物的情况下关闭供体部位(图12)。
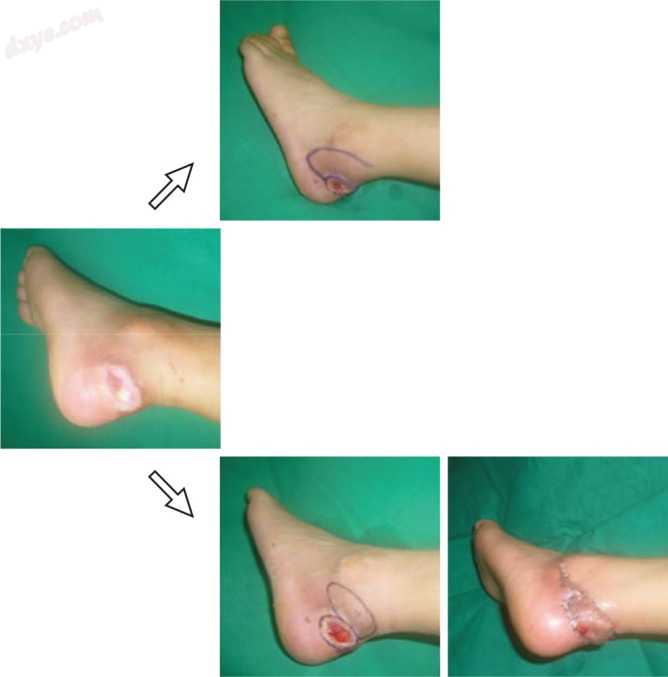
图12
传统设计与基于穿支的岛状皮瓣。传统设计的示例(上文)和基于基于穿支的岛状皮瓣(PBIF)(下文)的设计,用于重建跟腱的缺陷。由于以下几个原因,PBIF比传统的外侧跟骨瓣更容易接受:没有牺牲外侧跟骨血管,不需要皮肤移植,以及供体部位的初次闭合。
基于穿支的岛状皮瓣是穿支概念最成功的临床应用之一:基于穿支可以提升相同尺寸的皮瓣,而不需要牺牲源血管(16,31)。通过简单的设计和易于解剖以及供体部位的直接封闭(31),可以提升更具挑战性的岛屿皮瓣。此外,可以收获可靠的瓣,其可以充分旋转以覆盖缺损(24,25,37)。基于与缺陷相邻的多个穿支,可以快速可靠地采集PBIF,并且可以更有效地将收获的组织转移到缺损处(15,24)。
在重建手术中使用皮瓣已经从使用肌皮瓣到筋膜皮瓣,然后到穿支皮瓣,最后到基于穿支的岛状皮瓣。随机图案皮瓣是用词不当,因为他们的血液供应是由于外科医生不知道的微小穿支的存在而保留的,并且这种皮瓣实际上现在被认为是基于穿支的岛状皮瓣(1,15)。
此外,根据外科医生的创造力和能力,可提供各种类型和设计的皮瓣(1,16)。例如,患者在头颈部手术后在新食管处出现瘘管。为了重建瘘管,可以选择多种手术方式:局部皮瓣,如常规胸大肌岛状皮瓣,或游离皮瓣,如前臂皮瓣。在缺损附近检测到来自内部乳房血管的穿支,并且基于这些穿支设计了基于穿支的岛状皮瓣。皮瓣升高并转移至缺损部位,供体部位初次闭合(图13)。通过理解穿支(16)的结构,可靠性和功能(向皮瓣提供血管供应),使得PBIF的这种简单且有效的设计成为可能。穿支概念允许在穿支皮瓣(1,35)的设计中有效地使用组织。因此,外科医生可以减少外科手术提升皮瓣所需的时间和精力。熟悉穿支概念和技术的熟练外科医生可以获得优异的结果。
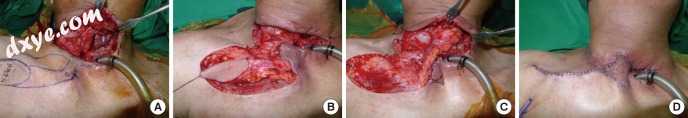
图13
基于穿支的岛状皮瓣。 (A)在新食道中形成的瘘管。 (B,C)基于乳房内血管的基于穿支的岛状皮瓣(PBIF)升高并翻转至缺损以修复食管瘘。 (D)供体点主要关闭。
结论
穿支皮瓣的引入代表了显微外科重建领域的重大进步。毫无疑问,穿支解剖对于初学者而言是一个繁琐的过程,涉及漫长而陡峭的学习曲线,并且需要在小蒂夹层中获得大量经验以及对解剖学知识的信心(1,16)。穿支的概念并不新鲜,但是从传统皮瓣的概念演变而来的想法。穿支概念允许以更可靠和更自信的方式收获和操纵皮瓣,即使在具有挑战性的情况下也是如此。穿支皮瓣与传统皮瓣相比具有多重优势(16)。薄皮瓣表面重修是可能的,并且可以很好地控制皮瓣的厚度,同时保留深的脂肪层。对于特定的外科手术重建,不再有任何“选择皮瓣”,因为特定手术组合物的“选择皮瓣”的常规供体部位已成为通用供体部位,从而允许在皮瓣的设计和组成中增加多样性和多功能性。此外,根据外科医生的技能和创造力,任何皮瓣都可以用作基于穿支的岛状皮瓣,其中源血管被完全保存。以这种方式,组织可以非常有效地用于定制和定制的重建(15)。
穿支皮瓣的使用是重建手术的新范例。穿支皮瓣与传统的皮瓣没什么不同,但它们确实取代了一些传统的皮瓣。因此,在给定的重建中长期持有的“选择皮瓣”的想法不再有效。然而,关于穿支的误解已经导致外科医生避免使用该技术而采用传统的皮瓣。因为在引入穿支概念之前进行的许多具有挑战性的重建包括类似于穿支皮瓣的皮瓣,后者最好被视为传统皮瓣的进化产品。
参考:
Perforator Flap versus Conventional Flap
1. Geddes CR, Morris SF, Neligan PC. Perforator flaps: evolution, classification, and applications. Ann Plast Surg. 2003;50:90–99. [PubMed] [Google Scholar]
2. McGregor IA, Morgan G. Axial and random pattern flaps. Br J Plast Surg. 1973;26:202–213. [PubMed] [Google Scholar]
3. Sinna R, Boloorchi A, Mahajan AL, Qassemyar Q, Robbe M. What should define a "perforator flap"? Plast Reconstr Surg. 2010;126:2258–2263. [PubMed] [Google Scholar]
4. Blondeel PN, Morris SF, Hallock GG, Heligan PC. Perforator flaps: anatomy, technique and clinical application. St. Louis: Quality Medical; 2006. [Google Scholar]
5. Taylor GI, Palmer JH. The vascular territories (angiosomes) of the body: experimental study and clinical applications. Br J Plast Surg. 1987;40:113–141. [PubMed] [Google Scholar]
6. Wei FC, Celik N. Perforator flap entity. Clin Plast Surg. 2003;30:325–329. [PubMed] [Google Scholar]
7. Wei FC, Mardini S. Free-style free flaps. Plast Reconstr Surg. 2004;114:910–916. [PubMed] [Google Scholar]
8. Grover R, Nelson JA, Fischer JP, Kovach SJ, Serletti JM, Wu LC. The impact of perforator number on deep inferior epigastric perforator flap breast reconstruction. Arch Plast Surg. 2014;41:63–70. [PMC free article] [PubMed] [Google Scholar]
9. Saint-Cyr M, Schaverien MV, Rohrich RJ. Perforator flaps: history, controversies, physiology, anatomy, and use in reconstruction. Plast Reconstr Surg. 2009;123:132e–145e. [PubMed] [Google Scholar]
10. Kim JT. New nomenclature concept of perforator flap. Br J Plast Surg. 2005;58:431–440. [PubMed] [Google Scholar]
11. Wei FC, Jain V, Suominen S, Chen HC. Confusion among perforator flaps: what is a true perforator flap? Plast Reconstru Surg. 2001;107:874–876. [PubMed] [Google Scholar]
12. Kang MJ, Chung CH, Chang YJ, Kim KH. Reconstruction of the lower extremity using free flaps. Arch Plast Surg. 2013;40:575–583. [PMC free article] [PubMed] [Google Scholar]
13. Agostini T, Russo GL, Zhang YX, Spinelli G, Lazzeri D. Adipofascial anterolateral thigh flap safety: applications and complications. Arch Plast Surg. 2013;40:91–96. [PMC free article] [PubMed] [Google Scholar]
14. Lee MJ, Yun IS, Rah DK, Lee WJ. Lower extremity reconstruction using vastus lateralis myocutaneous flap versus anterolateral thigh fasciocutaneous flap. Arch Plast Surg. 2012;39:367–375. [PMC free article] [PubMed] [Google Scholar]
15. Pribaz JJ, Chan RK. Where do perforator flaps fit in our armamentarium? Clin Plast Surg. 2010;37:571–579. [PubMed] [Google Scholar]
16. Kim JT. Latissimus dorsi perforator flap. Clin Plast Surg. 2003;30:403–431. [PubMed] [Google Scholar]
17. McGregor IA, Jackson IT. The groin flap. Br J Plast Surg. 1972;25:3–16. [PubMed] [Google Scholar]
18. Zayakova Y, Stanev A, Mihailov H, Pashaliev N. Application of local axial flaps to scalp reconstruction. Arch Plast Surg. 2013;40:564–569. [PMC free article] [PubMed] [Google Scholar]
19. Yoo KW, Shin HW, Lee HK. A case of urethral reconstruction using a superficial circumflex iliac artery. Arch Plast Surg. 2012;39:253–256. [PMC free article] [PubMed] [Google Scholar]
20. Han DH, Park MC, Park DH, Song H, Lee IJ. Role of muscle free flap in the salvage of complicated scalp wounds and infected prosthetic dura. Arch Plast Surg. 2013;40:735–741. [PMC free article] [PubMed] [Google Scholar]
21. Yoon SK, Song SH, Kang N, Yoon YH, Koo BS, Oh SH. Reconstruction of the head and neck region using lower trapezius musculocutaneous flaps. Arch Plast Surg. 2012;39:626–630. [PMC free article] [PubMed] [Google Scholar]
22. McCraw JB, Vasconez LO. Musculocutaneous flaps: principles. Clin Plast Surg. 1980;7:9–13. [PubMed] [Google Scholar]
23. Mathes SJ, Nahai F. Clinical atlas of muscle and musculocutaneous flaps. St. Louis: CV Mosby; 1979. [Google Scholar]
24. Yang J, Ko SH, Oh SJ, Jung SW. Reconstruction of a perineoscrotal defect using bilateral medial thigh fasciocutaneous flaps. Arch Plast Surg. 2013;40:72–74. [PMC free article] [PubMed] [Google Scholar]
25. Shin IS, Lee DW, Rah DK, Lee WJ. Reconstruction of pretibial defect using pedicled perforator flaps. Arch Plast Surg. 2012;39:360–366. [PMC free article] [PubMed] [Google Scholar]
26. Pontén B. The fasciocutaneous flap: its use in soft tissue defects of the lower leg. Br J Plast Surg. 1981;34:215–220. [PubMed] [Google Scholar]
27. Koshima I, Soeda S. Inferior epigastric artery skin flaps without rectus abdominis muscle. Br J Plast Surg. 1989;42:645–648. [PubMed] [Google Scholar]
28. Park JS, Roh SG, Lee NH, Yang KM. Versatility of the distally-based sural artery fasciocutaneous flap on the lower leg and foot in patients with chronic disease. Arch Plast Surg. 2013;40:220–225. [PMC free article] [PubMed] [Google Scholar]
29. Tan S, Lim J, Yek J, Ong WC, Hing CH, Lim TC. The deep inferior epigastric perforator and pedicled transverse rectus abdominis myocutaneous flap in breast reconstruction: a comparative study. Arch Plast Surg. 2013;40:187–191. [PMC free article] [PubMed] [Google Scholar]
30. Kimura N, Satoh K. Consideration of a thin flap as an entity and clinical applications of the thin anterolateral thigh flap. Plast Reconstr Surg. 1996;97:985–992. [PubMed] [Google Scholar]
31. Kim JT. Two options for perforator flaps in the flank donor site: latissimus dorsi and thoracodorsal perforator flaps. Plast Reconstr Surg. 2005;115:755–763. [PubMed] [Google Scholar]
32. Kim JT, Ng SW, Naidu S, Kim JD, Kim YH. Lateral thoracic perforator flap: additional perforator flap option from the lateral thoracic region. J Plast Reconstr Aesthet Surg. 2011;64:1596–1602. [PubMed] [Google Scholar]
33. Yang JD, Ryu DW, Lee JW, Choi KY, Chung HY, Cho BC, Park HY, Byun JS. Usefulness of a lateral thoracodorsal flap after breast conserving surgery in laterally located breast cancer. Arch Plast Surg. 2013;40:367–373. [PMC free article] [PubMed] [Google Scholar]
34. Jeong JH, Hong JM, Imanishi N, Lee Y, Chang H. Face reconstruction using lateral intercostal artery perforator-based adipofascial free flap. Arch Plast Surg. 2014;41:50–56. [PMC free article] [PubMed] [Google Scholar]
35. De la Parra M, Sanchez G, Lopez J, Perez A, Naal N. Total maxillary reconstruction using a double-barreled and double skin paddle fibular flap after total maxillectomy. Arch Plast Surg. 2013;40:779–782. [PMC free article] [PubMed] [Google Scholar]
36. Yoon TH, Yun IS, Rha DK, Lee WJ. Reconstruction of various perinasal defects using facial artery perforator-based nasolabial island flaps. Arch Plast Surg. 2013;40:754–760. [PMC free article] [PubMed] [Google Scholar]
37. Lazzeri D, Huemer GM, Nicoli F, Larcher L, Dashti T, Grassetti L, Li Q, Zhang Y, Spinelli G, Agostini T. Indications, outcomes, and complications of pedicled propeller perforator flaps for upper body defects: a systematic review. Arch Plast Surg. 2013;40:44–50. [PMC free article] [PubMed] [Google Scholar] |


