马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?注册
×
9.1简介
有时需要开腹治疗以挽救创伤和非创伤手术条件下的生命。血管外科医生需要了解腹部开放治疗的指导(见第5章),受伤区域和主要腹部血管的暴露(见第6章),以及血管外科手术中优选的临时腹部闭合方法。除了通常年轻患者的严重出血和相关腹内损伤的主要血管创伤后的损伤控制剖腹术和短期开腹治疗,长期开腹腹部治疗也是预防和治疗腹腔筋膜室综合征(ACS)的必要条件。 )老年人在修复破裂的腹主动脉瘤(AAA)后。损伤控制剖腹手术或缩短剖腹手术与第二次剖腹手术也可能是治疗腹部灾难患者(如急性中肠缺血(AMI)晚期)的有利策略。本章仅涉及非创伤性血管紧急情况下的腹部开放。
9.2修复破裂的AAA后腹部开放
9.2.1 AAA破裂后的腹腔筋膜室综合征
由于腹腔室综合征(ACS)引起的减压剖腹手术开始或开始或血管内修复破裂的AAA(RAAA)越来越频繁地进行。据报道,腹主动脉瘤破裂(AAA)开放性和血管内动脉瘤修复术(EVAR)后发生ACS的患者比例分别为30%左右[3]和20%。增加失血,低血压,大量液体复苏和主动脉长时间闭塞以及随后的内脏水肿再灌注损伤导致腹内高压或ACS的风险增加。围手术期坚持大规模输血方案,包装红细胞和血浆与血小板的比例为1:1:1,可降低ACS大量失控性出血的风险。如果在术后早期发现,可以用硬膜外镇痛,神经肌肉阻滞和利尿剂治疗腹内高压。这种积极主动的方法可以阻止ACS的发展。当ACS被确定为晚期或腹内压达到30 mmHg时,急救减压剖腹术是挽救生命所必需的。 AAA修复后对ACS的认识和及时管理对于改善ACS期间肠缺血的存活和发展至关重要,这与死亡率增加有关。
9.2.2决定让腹部开放时
在非创伤患者中,RAAA系列报告损伤控制剖腹手术患者的频率在5%到25%之间(表9.1)。 在13例患者的一份报告中,为了预防ACS,腹部通过真空包装技术暂时关闭,在RAAA修复后有或没有腹膜后包装。 这种损伤控制管理及早期决定使腹部保持开放导致早期ICU到达,用于对发现的休克,持续性凝血病,酸中毒和体温过低进行强烈复苏,死亡率为54%。

表9.1非创伤患者的一系列损伤控制剖腹手术中血管疾病的发生率
腹部开放的决定也可以在手术结束时进行:腹部可能只是保持开放,因为腹部可能无法闭合,例如,围手术期输液过量和腹腔肿胀。有时,外科医生开始将筋膜边缘缝合在一起但除去缝合线,因为闭合会导致腹部过紧和发生ACS的风险。筋膜闭合然后进行桌上腹内压力测量也可能导致筋膜缝合线的移除,从而允许完全腹部减压。由于继发性ACS的发展,在第二次手术后开腹修复后更常打开腹部。减压剖腹术可以直接进行或作为EVAR后的第二次手术进行。如果肠道,通常是结肠,缺血发展,与ACS共存的病症,也可以在EVAR后开放修复和剖腹术后进行再次切开术。
9.2.3长时间的腹部开放治疗可能是必要的
与年轻的创伤患者相比,老年AAA患者通常具有共存的合并症和受损的生理功能,例如心脏,肺和肾功能不全,导致相对治疗抵抗力,以减少通常在紧急修复后出现的液体超负荷。 RAAA。因此,在腹部闭合可能之前,开腹腹部治疗的持续时间通常会延长。因此,拥有一个耐用的敷料系统非常重要,可以最大限度地降低进一步并发症的风险并促进完全筋膜闭合。
9.2.4 AAA修复中的临时腹部闭合
在最近的系统评价中,最有效的TAC是AAA修复后的真空辅助伤口闭合和网状介导的筋膜牵引(VACM;图9.1):三项研究中的主要筋膜闭合率从96%到100%不等。在这三项研究中,开放腹部闭合的中位时间为10.5,17至36天。没有患有该技术的长期开腹腹部治疗的患者留下了计划的腹疝。移植物感染率为0%至6.7%。据报道,真空包装处理后报告的移植物感染率非常低,为0%至7.1%。在上文提到的前瞻性研究中,30名患者中有2名在采用VACM方法进行开腹腹部治疗后发生了大气压瘘。两者均有潜在的肠缺血,接受肠切除术并死亡。采用计算机断层扫描术,随访1年,15例患者中有9例出现切口中线疝。三个(20%)切口疝是有症状的,其中两个被修复。
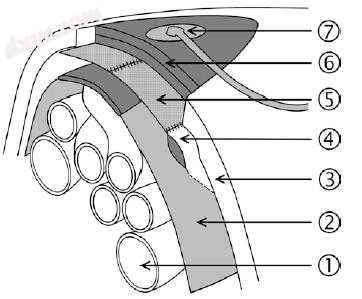
图9.1真空辅助伤口闭合和网状介导的筋膜牵引技术:1,肠; 2,内脏保护层; 3,腹壁; 4,腹壁筋膜; 5,聚丙烯网;如图6所示,将两片聚氨酯泡沫放置在网状物的顶部并在伤口边缘之间皮下;如图7所示,管道装置具有接口垫,该接口垫附接到自粘盖布中的开口并连接到真空源
在修复AAA后,VACM是治疗干净,IA级,开放腹部的良好替代方案。该方法即使在开放腹部治疗数周后也能促进高的原发性筋膜闭合率,因为这种NPWT联合技术和网状介导的筋膜牵引可抵消筋膜侧向收缩。在普通外科患者中已经复制了使用该技术实现高筋膜闭合率。一旦出现肠和/或感染性并发症,影响开腹的分级,主要延迟筋膜闭合率降低,肠瘘和移植物感染的风险增加。腹部开放治疗的持续时间似乎是一个关键因素,因为大多数严重并发症通常在2周后发生。
9.3急性肠系膜缺血管理后腹部开放
在急性肠系膜缺血中肠系膜动脉循环血运重建的使用越来越多,这使得对第二次或第三次剖腹探查的需求增加,用于评估肠道活力和肠道的确定性重建。在患有腹膜炎的患者中,损伤控制策略是明智的。在非创伤患者中,报告损伤控制剖腹手术的急性肠系膜缺血患者的频率在13%至31%之间(表9.1),这意味着急性肠系膜缺血是进行损伤控制剖腹手术时相当常见的原因。据报道,在一个系列的16名积极治疗的患者中,存活率为62%。血管和普通外科医生之间的合作可以改善结果。在最近制定的欧洲血管外科学会关于管理肠系膜动脉和静脉疾病的指南中,当肠道血运重建患者发生肠梗塞时,建议进行损伤控制手术和第二次剖腹手术。这种策略在非闭塞性肠系膜缺血和肠系膜静脉坏疽方面研究较少,但在这些急性肠系膜缺血实体中,自由使用第二次剖腹手术似乎也是一种合理的方法。
9.3.1急性肠系膜上动脉闭塞的治疗
最佳治疗可包括开放式和血管内手术,并且如果在合理距离内可获得,则最好在具有混合手术室的血管中心治疗患者。从术前临床和CT血管造影评估,可以确定患者是否患有腹膜炎以及闭塞是栓塞还是血栓形成。如果存在腹膜炎则通过检查肠的颜色,肠的扩张和蠕动,肠系膜动脉中的可见脉动和切割表面的出血来评估肠缺血的程度和严重程度,从而指示剖腹手术。急性肠系膜动脉血运重建,开放,混合或血管内,优选在任何肠道手术之前完成(图9.2)。 SMA和腹腔干的血运重建很少有任何迹象,其中SMA血运重建似乎更为重要和持久。在急性血栓性闭塞中,逆行开放肠系膜支架术可能是一种非常有用的混合方法,其中SMA暴露于剖腹手术,然后逆行再通血栓形成和动脉粥样硬化闭塞的SMA,并以逆行或顺行方式支架(图9.3)。所有初始紧急血管和必要的内脏手术都应在同一手术中进行。
9.3.2急性肠系膜缺血暂时性腹部闭合
当大部分肠道坏疽时,即使是低级别的腹内高压也可能致命。在这种情况下,重要的是优化剩余肠的灌注,这通常需要开腹治疗。在肠穿孔的情况下,受影响的肠段快速切除,然后进行肠系膜血运重建,留下肠道重建,直到18-36小时后进行第二次剖腹手术。急性肠系膜缺血患者的最佳TAC方法尚不清楚。虽然临时仅皮肤闭合可能是一些患者的良好选择,但在其他患者中可能需要完全开放的腹部来优化内脏循环。在一些报道中,由于继发性腹膜炎或需要肠切除和吻合的肠缺血导致的腹部长期NPWT是与肠大气瘘的发展和高死亡率相关的因素。值得注意的是,这些研究没有对照组。在最近对非创伤患者开腹和TAC技术的系统评价和荟萃分析中,与NPWT相比,NPWT连续筋膜牵引具有更高的延迟筋膜闭合率和更低的肠大气瘘形成率,强调了尽可能快地闭合腹部的有效方法,以减少与腹部开放相关的并发症的风险。
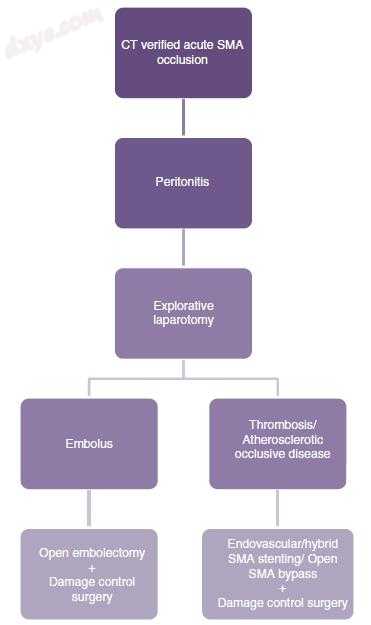
图9.2急性SMA闭塞和腹膜炎患者的流程图

图9.3逆行开放肠系膜支架术:用微针穿刺在SMA的主干上进行穿刺,并且通常用导丝将阻塞再通入主动脉。然后将近端SMA动脉粥样硬化闭塞与硬导管交叉,交换亲水导丝。这根导线在主动脉中被诱捕,使用通过股骨入口的圈套,然后将其带出,从而创建彻底通过访问。将导引器顺时针放置在SMA上,穿过股动脉的贯通导线,然后进行支架置入术
9.3.3延迟肠吻合术或造口
在第一次或第二次观察时,进行肠切除而无需重建。在接下来的剖腹手术中,会产生肠吻合或造口。在一个中心,产生临时造口,然后施用肠胃外营养直至手术恢复期结束。在进行广泛肠切除,近端切除空肠或多次切除的患者中,有效肠道血运重建后的肠吻合可能有利于避免高输出气孔,短肠综合征和与肠衰竭相关的死亡率增加。
带回家的消息
•修复腹主动脉瘤破裂后对腹腔室综合征的认识和及时处理对于提高生存率至关重要。
•对于需要长时间腹部开放治疗的患者,真空辅助伤口闭合和网状介导筋膜牵引是一种良好的临时腹部闭合方法。
•急性肠系膜上动脉闭塞和腹膜炎的患者应首先接受损伤控制剖腹手术,最好是肠道血运重建术。
参考:open abdomen a comprehensive practical manual |


