马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?注册
×
学习目标
• 熟悉Basyac囊性肾肿块分类系统
• 学习小肾脏肿块何时可忽略及何时应遵循
• 了解血管平滑肌脂肪瘤的超声、CT和MRI表现
• 了解非宏观脂肪性肾脏肿块的影像学表现
• 熟悉肾肿瘤分期及肾功能测定
• 了解肾癌患者治疗后的正常影像学表现及治疗和未治疗的转移性疾病的表现
• 了解靶向化疗药物治疗转移性肾癌的独特特征,包括免疫治疗
1.1 引言
1.2 肾脏占位性病变的影像学表现
1.2.1 超声波
虽然非对比超声评估囊性病变的内部形态比CT更详细,但它在检测或准确表征肾脏肿块CT或MRI方面并不敏感。大多数认为只有当诊断为一个简单的囊肿的肾肿块时,超声才是确诊的。
1.2.2 CT与MRI
肾脏肿瘤可在CT或MRI检查中偶然发现。在CT上,只有对比度增强图像是很常见的,在这种情况下,质量增强的评估是有限的。当仅对比增强CT图像可用时,可能难以区分高密度囊肿与实体低强化肾损害。肾癌在CT增强扫描上不可能超过70 HU,而CT增强扫描则不到40 HU。
近年来,有了很大的发展。
关键点
• 当延迟而不是早期对比度时获得最大的肾脏质量检测和表征 - 在造影剂注射开始后90-100s或排泄阶段[EP]中获得增强的图像(在肾脏相[NP]中, 当在肾脏收集系统中首次检测到排泄的造影剂时开始,通常在造影剂注射开始后120秒或更长时间)。
关键点
• 大多数良性和恶性非常小的肾肿块以相当慢的速度生长,其中许多肿块以每年最大直径不超过3-5mm的速度增大。 因此,肾脏肿块的间隔增大不能用于预测被跟踪的肿块是恶性的。 相反,群众应该评估形态的变化。 这些变化包括增加异质性或其他前述复杂特征的进展。
1.3 非常小的肾脏肿块(<1-1.5厘米)
在CT扫描的成人患者中,几乎有一半的肾脏肿块(最大直径<1~1.5厘米)。CT和MRI检测到的许多肾脏肿块由于其大小无法表征。准确的衰减测量在这些病变是有问题的,由于体积平均和假增强。幸运的是,这些病变中的任何一个是恶性的可能性非常低。这些病变绝大多数是良性肾囊肿。
由于非常小的肾肿块是如此常见,进一步评估所有这些病变是不可行的,即使少数将是癌症。
关键点
• 微小肾肿块的随访应在主观上表现为复杂的证据,表现为异质性、内隔膜、壁结节、壁增厚或异质性。
如果出现在高风险患者中,如具有已知或怀疑遗传性癌症综合征的患者(如von Hippel-Lindau,遗传性乳头状肾细胞癌,Birt-Hogg-Dubé或遗传性平滑肌瘤病 - 肾癌综合征)。 当一个非常小的肾脏肿块被认为可疑时,应在6-12个月内进一步评估。 可疑群众应至少追踪5年。 虽然可以通过CT或MRI进行随访,但MRI更准确。 即使是很小的囊肿也具有特征性的高T2信号强度。 MRI对比增强也比CT更敏感,并且不受伪增强影响。
1.4 囊性肾肿块
许多放射科医生和泌尿科医师使用波斯尼亚分类系统对囊性肾脏病变进行分类,该分类系统于1986年首次提出并多次修订,其中包括2005年。 该系统根据肾脏囊肿的恶变可能性将肾囊性肿块分为五类。 需要强调的是,Bosniak系统设计用于专用肾肿瘤CT,而不是用于超声或MRI。
I类病变,占绝大多数囊性肾肿块,是单纯性肾囊肿。它们是均匀的质量。它们是在超声上的消声和CT上的水衰减或MRI上的水信号强度。它们有不可见的壁,不含点状或钙化。当造影剂给药时,它们不会增强。I类病变总是良性的,不需要随访。II类病变最为复杂。它们可能包含一至三个间隔或薄的周边钙化。直径大于3 cm的肾囊肿也属于II类病变。II类病变基本上是良性的,不需要随访。IIF病变包括多个或增厚的隔膜,增厚的壁,或粗钙化。直径大于3 cm的高密度囊肿也是IIF类病变。
关键点
• IIF类囊肿已被发现代表癌症或进展成为癌症的约11%的时间,因此,必须降低,重复成像研究在6个月,然后每年至少5年。癌症应该被怀疑,而不是当这些病变随着时间的推移而增长,而是如果它们变得越来越复杂。
研究表明,这样的随访可以安全地形成。在亨德曼等人的系列报道中。17种IIF肾囊性肿块在最终随访期内均未发生局部复发或转移性疾病。Ⅲ类病变有增厚不规则增强的间隔或壁。它们在50到60%的时间内是恶性的。恶性时,他们往往不如其他肾癌。由于恶性肿瘤的高风险,通常建议治疗这些病变。Ⅳ类病变是囊性病变,有不规则的增强壁或增强结节。这些病变几乎总是恶性的,因此治疗是必要的。
Bosniak系统已被采纳用于超声和MRI; 然而,用这些方式恶性的不同类别病变的百分比并不为人所知。 例如,在MRI上,大约20%的囊性肾肿块显现得更加复杂,并且被分配到比用CT成像时更高的类别。 这主要是由于MRI能够检测CT不可见的内部囊肿特征。
一个小的回声性肾病例是癌症的可能性非常低。 在最近的一项研究中,随后发现161个小肾肿块中的1个(测量1 cm或更小)为肾癌。 在某些回声性AMLs之后已经发现声影,但不是在任何回声性肾癌之后。 在一些肾癌周围或在一些肾癌中观察到回声边缘或肿瘤内囊肿,但是没有观察到任何AML。
在美国上检测到的回声肿块常常用CT或MRI来评估,以确定肿块中是否存在宏观脂肪。如果在CT或MRI上鉴别出肉眼可见的脂肪,那么肿块就可以明确诊断为AML(只有可报告的例外情况)。
关键点
• 在CT上,肾组织内至少一些小区域的可视化(阴性)为10 HU或更低,被认为是对宏观脂肪和AML的诊断。
1.5 血管平滑肌脂肪瘤(AMLs)
AMLs是最常见的良性固体肾肿瘤。 它们由不同的相对分布的血管瘤,肌瘤和脂肪成分组成。 百分之八十发生偶尔。 其余与综合征(结节性硬化症或淋巴管瘤 - 肌肉瘤病)有关。
虽然几乎所有的AMLs在超声上都是回声的,一些小肾癌也是如此。然而,已经发现。
关键点
• 在MRI上,脂肪通常具有较高的T1和T2信号,并在脂肪抑制时丢失信号。 在反相化学位移成像中,AML中脂肪 - 水界面以及AML和相邻肾组织之间存在特征性的“印度油墨”伪影(图1.1)。
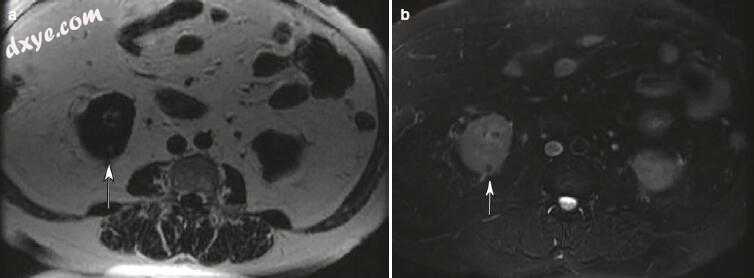
图1.1 AML的MRI。 (a)轴位T1加权MR图像显示右肾下极(箭头)有微小的高信号。 (b)具有脂肪抑制的轴位T2加权MR图像显示损伤已经失去信号(箭头),确认诊断。 (c)反相 - 相MR图像显示在肾脏与肾脏的界面处的(箭头)
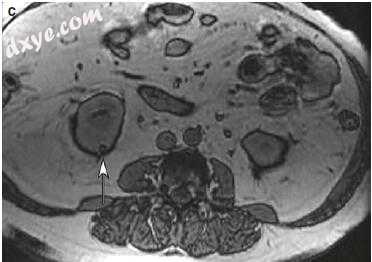
图1.1(续)
有时,外生AMLs可能难以区分与肾周脂肪肉瘤。一些成像特征可以用来促进分化。AMLs更容易进入肾脏并产生灶性实质缺陷。相比之下,脂肪肉瘤仅仅压迫肾脏,而没有相关的缺陷。AMLs更可能包含延伸到肾皮质的大血管,而不是脂肪肉瘤。
一些AML不包含容易识别的宏观脂肪。这些AML被称为脂肪贫血症AMLs(FPAMLs),包括FPAMLS,其与未增强CT和AMLs与上皮囊肿(AMLEC)具有相同或更高的衰减,其可表现为具有小囊性区域或多房囊性病变的实性肿块。
许多研究试图确定脂肪小灶或其他影像学特征,可能允许fpAMLs与其他实性肾肿瘤正确区分。 这些特征包括评估未增强的CT质量衰减,CT直方图,定量评估MRI上的脂肪,以及增强质量的程度和均匀性。 结果混杂。 例如,一些fpAMLs比正常肾实质具有更高的增强衰减,但乳头状肾癌也可以表现出这种特征。 一些fpAML在T2加权MR图像上信号强度低,但乳头状肾癌也可能表现出这种行为。 幸运的是,fpAMLs通常表现出比乳头状肾肿瘤更多的MR对比增强,因此在MRI上显示非增强CT上高度衰减和/或低T2信号强度的高血管病变最可能是AML。
一种罕见类型的AML是上皮样AML(EAML)。一些上皮样AML表现出积极性。它们可在局部扩散以侵犯肾静脉或IVC,累及局部淋巴结,甚至远处转移。Epithelioid AMLs没有展示允许它们与其他AML分化的成像特征。虽然许多上皮样AML不包含可识别的宏观脂肪在成像研究中。
1.6 其他肾实质肿块
许多肾实质肿块不包含可识别的脂肪。这包括嗜酸细胞瘤和肾癌。大量的研究试图区分各种非脂肪或最低脂肪的固体肾脏肿块在CT和MRI上取得了有限的成功,然而,一些偶尔暗示成像特征已被描述。
1.6.1 嗜酸细胞瘤
嗜酸细胞瘤是良性的肾脏肿瘤。它们可能包含可以在成像研究中检测到的中央疤痕;然而,这个特征不是诊断的。肾癌坏死与嗜酸细胞瘤的瘢痕不可区分。此外,大多数CT评价的嗜酸细胞瘤不包含可见的中央瘢痕。一些被用于区分癌细胞瘤的特征之一是节段性增强反转,其中两种不同增强的成分在CMP图像上识别其在EP图像上的衰减,其初始衰减更高,并且快速增强COMPO。NTEN在衰减上比初始低衰减和低强度增强分量低。这种特征在嗜酸细胞瘤中不被一致地检测,因此常常是没有帮助的。
1.6.2 肾癌
在过去,人们认为只有少数类型的癌症,然而,染色体分析表明,至少有13种不同类型的肾癌,其中最罕见的。包括透明细胞(约70~80%)、乳头状(10-15%)、不染色细胞(小于10%)、获得性肾囊性疾病、透明细胞和乳头状结合、集合管、肾髓质、粘液性管状和梭形细胞、琥珀酸脱氢酶缺乏、肾小管囊肿和UNCL。恶性肿瘤,多房囊性肿瘤的低恶性潜能,以及MIT跨位置的癌症,包括XP11.2。肉瘤样肾癌不再被认为是一种独特的细胞类型。相反,任何类型的原发性肾肿瘤可以去分化和发展肉瘤样特征。虽然大多数肾癌之间的成像分化是不可能的,但一些细胞类型倾向于显示某些成像特征,如下所述。
1.6.2.1 肾透明细胞癌
透明细胞肾癌具有最高的转移潜能和最主要的组织学RCC亚型的最差生存率。它们通常是异质性肾皮质肿块。在未增强的MRI上,大多数透明细胞癌在T2加权图像上表现出高强度。由于丰富的细胞内脂肪,透明细胞癌可能会失去信号相反的相位梯度回波T1加权图像。透明细胞癌通常表现为异质性增强,在CMP图像(图1.2)早期出现峰值增强。
1.6.2.2 乳头状肾癌
大多数乳头状癌比透明细胞癌表现出较少的攻击性。对比增强CT或MRI,乳头状癌倾向于均质。在未增强CT中,它们可能比邻近的肾实质具有更高的衰减。在未增强MRI上,它们往往在T2加权图像上是低值的,并且由于存在含铁血黄素而在同相T1加权图像上可能失去信号。它们通常比其他肾癌更均匀、更慢,并在较小程度上增强,直到NP甚至EP(图1.3)才发生峰值增强。

图1.2透明细胞肾细胞癌。 在CMP期间获得的增强的轴向(a)和冠状(b)图像显示出异质且活跃增强的左肾肿块,随后证实其为透明细胞RCC
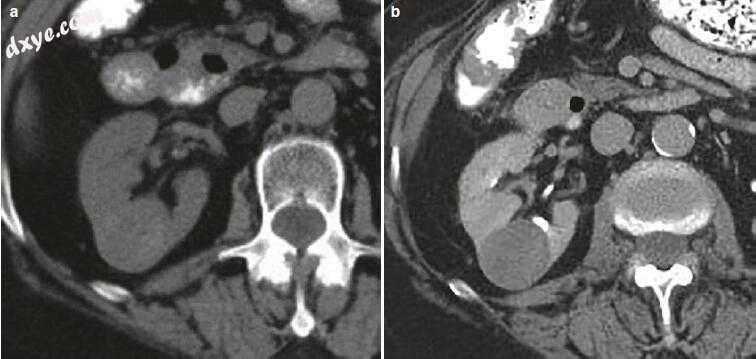
图1.3乳头状肾细胞癌。 未增强(a)和未增强(EP)对比增强(b)轴向CT图像显示中右肾后部方面的轻度不均匀增生性乳头状癌
1.6.2.3 嫌色细胞性肾癌
嫌色细胞性肾癌通常是分化良好的癌症,只要没有肉瘤样变性,生长缓慢,预后良好。它们在成像研究上没有独特的外观,不能可靠地区别于不包含宏观脂肪的其他实体肾肿块。
1.6.2.4 罕见的肾癌细胞类型
许多罕见的肾癌没有暗示的影像学表现。然而,一些关于这些癌症的具体评论可以被提出。肾髓质、集合管和XP11.2易位癌通常在肾髓质中出现。收集管癌在老年人中经常发生,肾髓质和XP11.2癌通常在年轻患者中遇到。肾髓质癌通常在镰状细胞特征的患者中发展。
1.6.3 尿路上皮肿瘤,淋巴瘤和肾动脉瘤
有时可以很难区分中心定位的RCC和尿路上皮癌;然而,在许多情况下,可以预测正确的病因。与RCC不同,尿路上皮癌在肾集合系统中具有中心,可产生肾盂充盈缺损,并倾向于保持正常的肾轮廓。他们也很少包含囊性/坏死的区域,在许多,但不是全部,RCCs。其他中心位置的肾脏肿块,可能会遇到和偶尔模仿尿路上皮癌的RCC包括肾淋巴瘤和肾动脉瘤。
1.7 肾实质质量增长率
良性和恶性实体肾肿块可以保持稳定的大小或随着时间的延长,两种类型的病变的生长率通常同样缓慢。有人建议,在至少5年的时间内,平均生长速率小于3毫米/年且形态没有改变的小固体质量应该被认为是稳定的。这种病变,即使恶性,也极不可能转移。相反,肿块的快速生长(在12个月内超过5毫米)可能表明攻击性/恶性。
1.8 放射组学
近年来,计算机辅助诊断(CAD)在检测和表征泌尿生殖系统异常方面的应用越来越受到人们的关注。关于肾脏肿块,这是以计算机辅助技术区分不同类型肾肿块的能力为中心的。例如,使用计算机辅助诊断的研究已经证明透明细胞肾癌具有比乳头状肾癌或AML更大的客观异质性(像素标准偏差、熵和均匀性)。CAD检测峰值病变衰减的差异也被用来区分透明细胞肾癌与其他肾肿瘤的一些成功。肾质量灌注参数已被用来区分一些肾肿瘤的高弗尔曼级与低年级。这些结果是有希望的,但初步的。
1.9 成像在肾实质分化中的应用
关键
• 由于主观检测到的许多影像学检查结果与使用CAD的重叠,目前许多恶性肿瘤与良性无脂固体肾肿块(或各种恶性实性肾肿块之间)的成像分化是不可能的。
1.10 肾脏经皮穿刺活检
鉴于许多肾脏病变的成像特征的重叠,经皮活检对于确定许多肾脏肿块在治疗前的性质是必需的。 活检可以准确而安全地进行。 针道播种肿瘤的风险很小。 只有孤立的肾癌播种病例报告。 活组织检查的一个潜在缺陷涉及只有少部分肾脏样本被采样的事实。 含有高等级癌症的区域可能无法取样,导致低估肿瘤侵袭性。
1.11 肾癌预处理评估
1.11.1 分期
在肾癌分期中,CT和MRI(在增强的门静脉期获得)至少90%准确,TNM分期系统如下:
阶段 特点
T1a 最大直径≤4厘米,限于肾脏
T1b > 4-7厘米,限于肾脏
T2a 7-10厘米,限于肾脏
T2b > 10厘米,限于肾脏
T3a 延伸到肾静脉或其分支或侵入肾周或肾窦脂肪
T3b 进入隔膜下方的IVC
T3c 进入隔膜上方的IVC或侵入IVC壁
T4 侵入超过肾周围筋膜或进入同侧肾上腺
N0 没有淋巴结受累
N1 区域淋巴结受累
M0 没有远处转移
M1 远处转移
Mx 未确定远处转移状态
在阶段性肾癌中成像的最大实际限制是由于CT和MRI难以确定肾癌是否已经侵入肾囊并且扩散到肾周或肾窦脂肪(从T3癌中区分T2)。 肾周软组织绞痛可由肿瘤,水肿或血管产生。 建议只有在肾周空间中发现结节性组织时,才能在CT或MRI上诊断出T3疾病。
1.11.2 肾脏肾功能测定
许多泌尿科医师倾向于在手术前获得怀疑或已知肾癌的RENAL肾功能评分。 肾脏测量评分允许泌尿科医生预测可以有效且安全地进行部分肾切除术的可能性。 使用该系统,肾脏肿块可以获得1-3分的评分(肾脏肿块大小,外部生长率,肾脏收集系统的临近度,前部或后部位置以及相对于上部和下部极线的位置) (见下表);复合肾功分数为4-6分的肿瘤被认为非常适合于肾部分切除术,而分数为10〜12分的肾部分肾切除术患者不适合进行全肾切除术。 后一组。
1.12 肾癌管理
目前尚未转移到区域或远端的肾癌的管理范围从主动监测(对于伴有显著并发症的老年患者的小[<4 cm]惰性(低Fuhrman等级)肿瘤)到热消融,部分肾切除术或完全肾切除术。 积极监测的患者应每6个月进行一次随后的影像检查一年,然后每年进行一次影像检查至少5年。 只有当肿块大小超过4厘米或每年增长大于5毫米时才考虑对这些患者进行干预。
1.13 肾癌治疗后的成像
1.13.1 肾脏消融或切除术后
成功的肾脏射频或冷冻消融后,消融部位有初始扩张。 最初,在消融床中可以正常检测到一些增强,特别是在MRI检查中。 这种正常的增强会随着时间而解决。 在消融后的几个月内,消融床通常会减少,但很少完全消失。 其他正常的消融后发现包括消融床与正常肾实质和周围晕圈之间的脂肪内陷,这些变化造成可与AML混淆的外观(图1.4)。 消融床扩张通常不会在微波消融后出现。
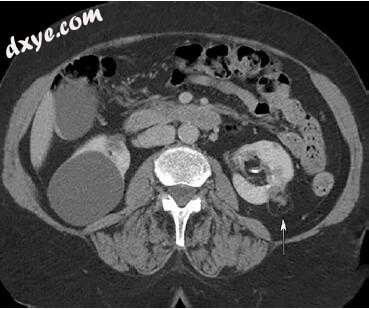
图1.4正常的热后消融外观。 7个月前进行左肾射频消融的患者的EP对比增强CT图像显示正常的消融后外观。 软组织衰减材料被内陷的肾周脂肪包围,该外观可与AML混淆
关键
• 频繁成像应在消融后进行(例如,在1,3,6和12个月)。 这是因为残留或复发肿瘤通常在消融的前几个月内可检测到。
如果消融床逐渐增大(而不是减小),当肾周结节增加时,或者当检测到结节或新月体增强的持续或新的区域时,应该在消融后怀疑持续性或复发性肿瘤,通常这些区域通常位于消融床与相邻肾实质的界面处。
1.13.2 部分或全部肾切除术后的影像
部分或全部肾切除术后,常见的术后炎性或纤维化改变在手术床,以及肾轮廓在部分肾切除术部位的畸形。Gore Tex网沿肾切除术部位呈沿肾缘高衰减的线性区域。
关键点
• 经常使用的止血材料可被误认为是感染或肿瘤,因为材料内的偶尔气体和其低衰减成分可在手术后持续数月。
肾部分切除术后并发症的发生率明显高于全肾切除术后,包括假性动脉瘤、尿路瘤或脓肿等并发症。如果尿毒症是一个问题,延迟造影>1 - 2小时后对比剂可能证明有用的文件尿漏。
部分或全部肾切除术后,复发性肿瘤可在手术床和/或局部或远处发展。外科手术复发可能最初难以区分术后瘢痕/纤维化,虽然肿瘤往往表现出可检测的增强和扩大随着时间的推移。肾癌通常转移到局部淋巴结、肝脏、肾上腺、肺和骨骼。肾上腺癌转移的透明细胞肾癌可能是有问题的,因为它们可能含有大量的细胞内脂肪。结果,与腺瘤相似,肾上腺转移瘤在相反的MR图像上表现出低信号强度,并且在延迟增强CT上也显示出明显(>60%)的洗脱。肾癌比其他肿瘤更常见于胰腺转移。
1.13.3 转移性疾病的影像学治疗
1.13.3.1 RECIST
患有或发展为转移性肾癌的患者必须接受系统治疗。然后定期进行影像学检查,以确定患者是否对化疗有反应。然后测量和比较转移病灶,从一项影像学研究到下一项。最常用的评估肿瘤化疗反应的测量系统一直是实体瘤(RECIST)系统的反应评估标准。 RECIST 1.1系统涉及多达5个转移性病变的测量(每个器官不超过两个,每个测量的病变长度至少为10mm)。大多数转移瘤是以最大尺寸测量的;然而,在短轴直径上测量淋巴结。在随访成像中所有转移瘤均得到解决时,诊断为完全缓解。当一项研究到下一项研究中所有目标病变总和减少≥30%时,诊断为部分缓解。当所有目标病变的总和增加≥20%或更多时,诊断为进展性疾病。在30%减少和20%增加之间的任何变化被认为是稳定的疾病。
关键点
• 虽然RECIST 1.1对于通过先前的标准化学疗法治疗的转移性疾病后效果良好,但其在用抗血管生成药物(包括多激酶抑制剂)治疗的患者中使用时存在问题。 这是因为多重激酶抑制剂可能在反应性转移病灶中产生坏死(并且造影剂CT上减弱的衰减),而没有这些病灶的大小显著减小。 因此,如果仅使用RECIST,那么作为部分响应者的患者可能被错误地认定为没有对治疗做出响应。
1.13.3.2 多激酶抑制剂
已经设计了许多替代的测量系统,它考虑到损伤衰减的变化以及尺寸的变化。这包括Choi,改进的Choi,以及形态、衰减、尺寸和结构(质量)系统。根据CII准则,例如,靶病变大小仅为10%或更多或目标衰减为15%或更多的减少指示部分响应。用修改后的CUI标准,这两个特征必须同时存在。
1.13.3.3 免疫治疗
在过去的几年中,转移性肾癌患者接受了免疫治疗。 这些药剂是靶向于攻击淋巴细胞上的受体或肿瘤细胞上的表面配体的抗体。 它们通过干扰肿瘤抑制免疫应答的能力而起作用。 目前,被抑制的免疫检查点包括与细胞毒性T淋巴细胞相关抗原4(CTLA4)和T细胞上的程序性细胞死亡蛋白1受体(PD-1)或其相关配体有关的那些 肿瘤细胞(PDL1和PDL2)。
关键点
• 免疫疗法治疗转移瘤的一个独特特征是,如果使用RECIST 1.1,一些反应性病变最初可能会出现稳定甚至扩大至可诊断进展性疾病的程度。 规模明显增加应被视为未经证实的进展性疾病(UPD)。 UPD必须在不少于4周内通过另一项随访影像学研究证实。 如果转移继续扩大,则可以诊断出进行性疾病。 然而,在一些情况下,随后的研究将显示肿瘤反应(由减小的大小和/或减弱组成),确认大小的初始变化仅仅是“伪进展”(图1.5)。 用于评估免疫治疗患者转移性肿瘤的系统已经修改,以考虑到这个问题(iRECIST标准)。
免疫疗法治疗转移性肾癌的疗效初步研究是有希望的。许多患者有持续的反应,甚至在治疗停止后仍然存在。
1.13.3.4 多激酶抑制剂治疗与免疫治疗的并发症
在接受新体系治疗的患者中遇到的并发症包括6周后获得的肝脂肪变性,胆囊炎,胰腺炎,肠穿孔和动脉血栓形成。 (c)现在又一个4周后进行的一项随访研究显示,肿块在坏死和较小(多激酶治疗后)和结肠炎(节段性或弥漫性),肺炎和皮炎以及少见的甲状腺炎,垂体炎,胰腺炎 ,和肾上腺功能障碍(免疫治疗后).

图1.5免疫治疗后肾上腺转移。 (a)初始增强CT图像显示左肾上腺大量肿块。 (b)质量仍然不均匀,在随访CT上更大
1.14 结束语
过去几年来,对肾实质肿块的影像学、诊断和治疗有许多令人兴奋的新进展。这包括识别的图像特征,可以区分一些囊性和固体肾肿块。不幸的是,在许多患者中,重叠的特征仍然阻止肾癌与良性肾损害的区分。由于这个原因,活检可以安全地进行,而不关心肿瘤播撒,通常用于诊断。成像对于肾癌的分期仍然是至关重要的,因为它是非常准确的。在器官-局限性疾病患者中,影像学可以用来确定哪些患者是部分与全肾切除术的候选者。越来越清楚的是,一些小的肾恶性肿块患者可能不需要治疗。新的化疗药物已经大大延长了局部或远处转移性疾病患者的存活率。用新靶向药物治疗后的肿瘤反应可以维持,但有时会延迟。肿瘤坏死无大小减少,偶尔可见,不应混淆与缺乏反应。
参考:Diseases of the Abdomen and Pelvis 2018-2021 Diagnostic Imaging - IDKD Book |


