- 快捷导航 |



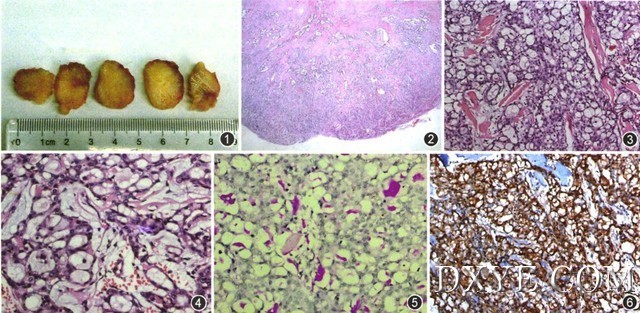 图1乳腺肿块切面灰白,质硬,有黏滑感;图2乳腺分泌性癌,肿瘤境界清楚,无包膜,纤维间质硬化HE低倍放大;图3肿瘤细胞形成微囊结构,囊内见粉红色分泌物HE中倍放大;图4细胞核圆,核仁可见,胞质颗粒状HE高倍放大;图5肿瘤细胞内外均可见红色分泌物PAS染色高倍放大;图6肿瘤细胞胞核S-100蛋白呈阳性表达EnVision-plus法 中倍放大 患者男,15岁。因8年前发现左乳1.5 cm肿块,近年来肿块逐渐增大伴轻微压痛于2013年7月10日就诊。体格检查:距左侧乳头0.5 cm处乳晕下方触及肿块,质地硬,与周围境界清楚,活动度好,轻微压痛,无乳头溢液,皮温正常。患者无外伤史,无乳腺癌家族史,无男性乳腺发育症,同侧腋窝淋巴结未触及肿大。B超示:左乳乳头后方见一不均质低回声区,大小2.3 cm×2.0 cm×1.6 cm,边界尚清,周边及内部见较丰富血流信号。术中见肿物与周围乳腺组织境界尚清,行肿块单纯切除术。 病理检查:灰黄灰白色肿物组织一块,大小2.5 cm×2.2cm×1.0 cm,结节状,无明显包膜。切面灰白,质稍硬,有黏滑感(图1)。镜下观察:肿瘤细胞排列成腺样和岛屿状,并形成大量筛孔及微囊样结构,囊内见分泌物。细胞圆形,中等大小,可见小核仁,胞质丰富淡染,呈颗粒或空泡状。 核分裂象偶见(在所有切片中见2个核分裂象)。肿瘤中央纤维间质硬化,分隔肿瘤细胞使之略呈放射状。周围肿瘤细胞更为丰富,似有边界,但无真性包膜,未见导管原位癌成分(图2~4)。PAS特殊染色,可见细胞内及细胞外呈现红色分泌物(图5)。免疫组织化学染色结果:肿瘤细胞S-100蛋白(图6)、CD117、CK8/18均为阳性,雌激素受体、孕激素受体、HER2、GCDFP-15、癌胚抗原(CEA)均为阴性,Ki-67阳性指数约2%。 病理诊断:(左乳头下方)乳腺分泌性癌。 讨论: 乳腺分泌性癌(secretory carcinoma of breast),又称幼年性乳腺癌(juvenile breast carcinoma),是首先由McDivitt和Stewart。在1966年总结分析了7例乳腺癌儿童患者的资料后提出的概念,此型乳腺癌具有独特的形态学特征,后发现在成人中亦可发生,结合其组织学特征命名为分泌性癌2,在2012年版WHO乳腺肿瘤分类中已作为独立类型归为罕见类型和变异型。该类型占所有乳腺癌的比率<0.15%,可见于男女患者,是儿童乳腺癌中最常见的类型。 我们检索国内外发生于男童的报道有19例,本例作为新增1例,为进一步了解此类疾病提供参考。乳腺分泌性癌的肿瘤大小平均3 cm,境界清楚,无纤维包膜,可出现浸润性生长方式,肿瘤细胞可排列成不同比例的实性、微囊和管状结构,其间被硬化性纤维间质分隔,细胞轻度异型,胞质呈颗粒状或空泡状,核圆形,核仁清晰,罕见核分裂象。该类型肿瘤可伴坏死或周围伴导管原位癌成分,本例未见以上病变。PAS特殊染色显示细胞内和细胞外分泌硫酸黏多糖。分泌性癌需与泌乳性腺瘤、富于脂质癌、黏液性癌、腺泡细胞癌鉴别,主要根据细胞核的异型性及细胞分泌物PAS染色结果进行判定。 研究显示分泌性癌的遗传学特征表现为t(12,15)染色体发生易位,ETV6一NYRK3基因融合,在儿童恶性间叶性肿瘤亦可见此基因的融合,另外,分泌性癌的免疫表型与基底样型乳腺癌相同,提示两者的基因突变有重叠。 目前的研究显示,绝大多数分泌性癌患者预后良好,国内学者总结了一些预后不良的因素,但男童分泌性癌患者的预后及治疗方案尚未统一。本例经上海复旦大学附属肿瘤医院会诊后,行保乳头肿块周围扩大切除及同侧腋窝淋巴结清扫,肿块周围乳腺组织和腋窝淋巴结18枚均未见癌累及,此与文献报道的较少发生腋窝淋巴结转移相一致,我们将密切随访,完善病史,为儿童分泌性癌的治疗提供进一步的临床经验。 |