马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?注册
×
,内镜胆囊引流手术,包括内镜经乳头胆囊引流术 (ET-GBD) 和内镜超声引导胆囊引流术 (EUS-GBD) 已成为替代治疗选择(图 1)。ET-GBD 涉及将支架从十二指肠通过大乳头和胆总管放入胆囊,适合可能需要同时进行 ERCP 的胆总管结石或胆管炎患者。然而,ET-GBD 在识别和插管曲折的胆囊管方面面临许多内镜技术挑战,特别是在结石负担较大的情况下。
图 1。
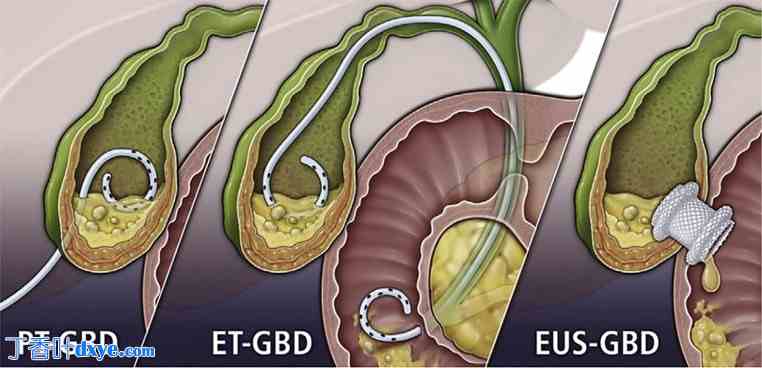
胆囊引流手术包括经皮胆囊造口术 (PC)、内镜经乳头胆囊引流术 (ET-GBD) 和 EUS 引导的 GBD (EUS-GBD)。
在 EUS-GBD 中,胆囊在 EUS 引导下直接排入胃(胆囊胃造口术)或十二指肠(胆囊十二指肠造口术)。LAMS 已成为首选支架,因为它们简化了电灼增强部署和哑铃形设计,改善了胆囊和肠壁的贴合,减少了泄漏、穿孔和支架移位。LAMS 的短而宽的鞍座(10-15 毫米中段)减少了结石、污泥和碎片对支架的阻塞,并允许通过 LAMS 进行各种额外的治疗操作,包括胆囊镜检查、结石提取、碎石和息肉切除术。由于这些独特的特性,LAMS 可用于内窥镜检查胆囊引流术是手术风险高的患者、经皮引流术失败或姑息情况下的首选。例如,作者展示了一例使用 LAMS 进行 EUS-GBD 的成功案例,该案例中的患者患有急性胆囊炎,由于广泛的肝转移而无法进行经皮引流(图 2)。
图 2。
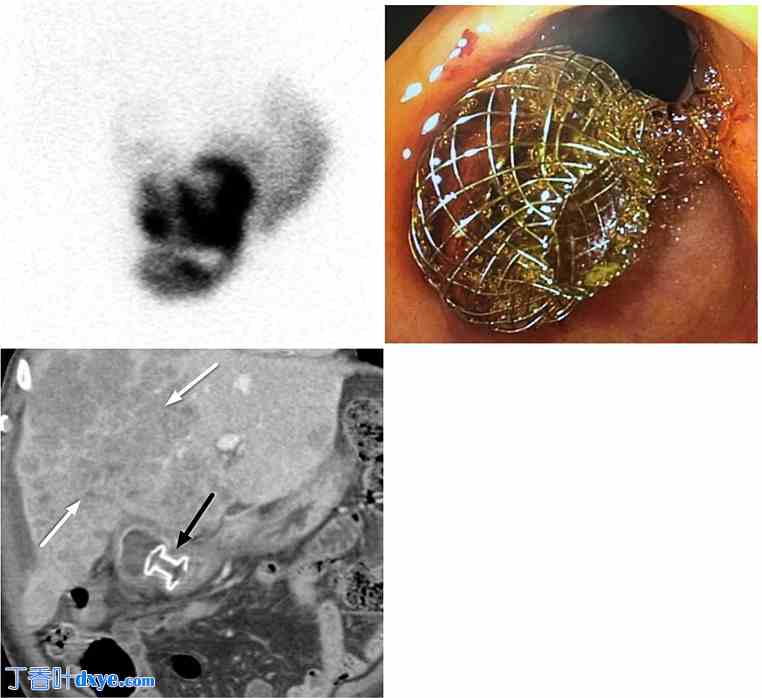
79 岁男性,患有前列腺癌,不适合手术,出现急性胆囊炎和克雷伯菌血症。A. 4 小时的 HIDA 扫描显示胆囊中没有示踪剂排泄,诊断为急性胆囊炎。B. 胃窦内窥镜图像显示 LAMS 胆囊胃造口术是作为手术和经皮胆囊造口术的替代方案进行的。 C. 对比增强冠状 CT 图像显示广泛的肝转移(白色箭头),无法进行经皮引流。内镜胆囊胃造口术利用 LAMS(黑色箭头)成功实施,作为一种治疗替代方案
胆囊内 LAMS 的最佳留置时间尚未确定。除非胆囊管阻塞得到解决,否则从胆囊中移除 LAMS 通常会导致胆囊胃造口自发闭合和复发性胆囊炎。另一方面,如果支架无限期地留置,可能会发生支架移位或胆囊壁侵蚀性损伤以及胆囊/胃/十二指肠壁出血。据报道,长期放置支架(长达 3 年)没有发生与支架相关的不良事件。有传闻称植入时间更长,没有不良事件,例如作者已经证明的(图 3)。
图 3。
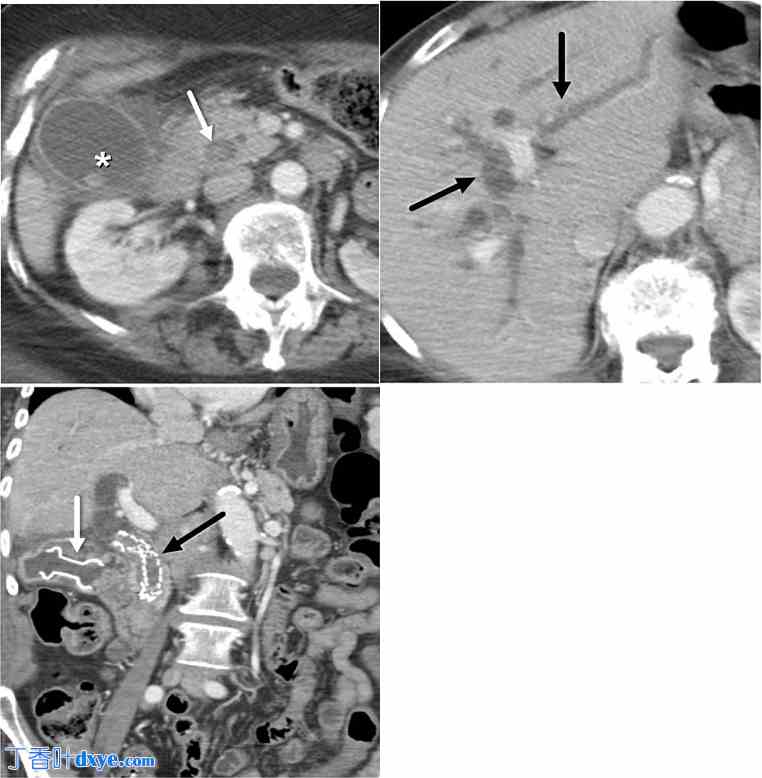
86 岁女性,因胆总管结石并发急性胆囊炎和上行性胆管炎而就诊。A. 增强轴向 CT 图像显示胆结石、胆囊壁增厚和急性胆囊炎胆囊周围积液(白色星号),并发胆总管结石引起的上行性胆管炎(白色箭头)。B. 增强轴向 CT 显示中度双叶肝内胆管扩张(黑色箭头)。C. 增强冠状 CT 图像显示 LAMS(白色箭头)将胆囊引流到十二指肠,并且在同一次 ERCP 过程中放置了胆道支架(黑色箭头),该患者不适合手术。胆道支架和 LAMS 均保留了 5 年。患者随后又发作了一次胆管炎,最终因无关原因去世,享年 92 岁
虽然多项回顾性队列研究和荟萃分析表明,内镜胆囊引流技术(ET-GBD 和 LAMS EUS-GBD)和 PC 的技术和临床成功率相当,但内镜胆囊引流技术已显示出较低的不良事件发生率和改善的生活质量 [15–20]。Teoh 等人的研究表明,30 天不良事件(12.8% vs. 47.5%)和复发性胆囊炎(2.6% vs. 20%)显著减少。
随着 LAMS 在内镜胆囊引流中的应用越来越广泛,并得到 FDA 的批准,放射科医生应注意其各自的相关风险、禁忌症和并发症。一项包括 393 名使用 LAMS 进行 EUS-GBD 的患者的荟萃分析显示,总体不良事件发生率为 12.7%,包括出血、支架移位、支架阻塞、复发性胆囊炎或胆管炎、胆漏、穿孔(十二指肠或胆囊)和死亡(图 4)。EUS-GBD 的禁忌症之一是坏疽性或穿孔性胆囊炎,因为泄漏风险增加,并且由于胆囊壁易碎而形成脓肿(图 5)。对于未来可能接受肝移植的内镜胆囊引流术候选人来说,一个重要的考虑因素是,ET-GBD 是该群体的首选,因为它可以保留胆囊的天然胆道解剖结构和结构完整性。由于这些原因,建议考虑进行内镜胆囊引流术的患者接受多学科评估。
图 4。
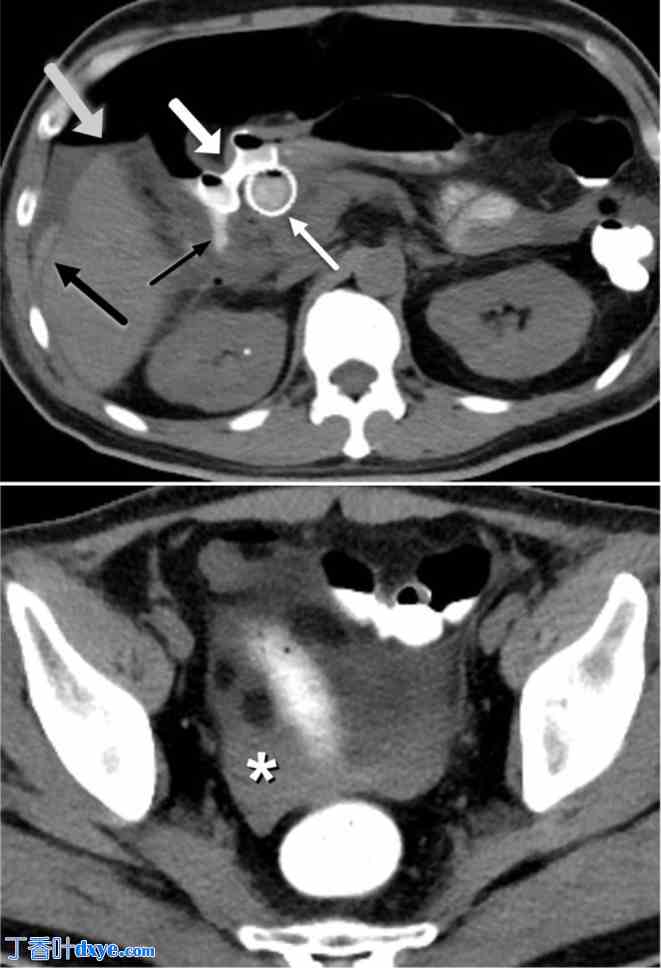
73 岁男性,患有胰腺癌和急性胆囊炎。A. 轴向 CT 图像显示 LAMS-胆囊胃造口术(粗白箭头),旨在缓解急性胆囊炎。Axios 明显从胆囊中移位或移位,在肝周间隙中观察到口服造影剂(粗黑箭头),以及气液平面(灰色箭头),表明存在气腹和腹水。观察到 LAMS 远端部分的腔外造影剂泄漏(细黑箭头)。在 CBD 中观察到含有造影剂和少量空气的胆道支架(细白箭头)。 B. 轴向 CT 图像显示盆腔腹水中的液液平面表明存在外渗的口服造影剂与液体混合(白色星号)
图 5。
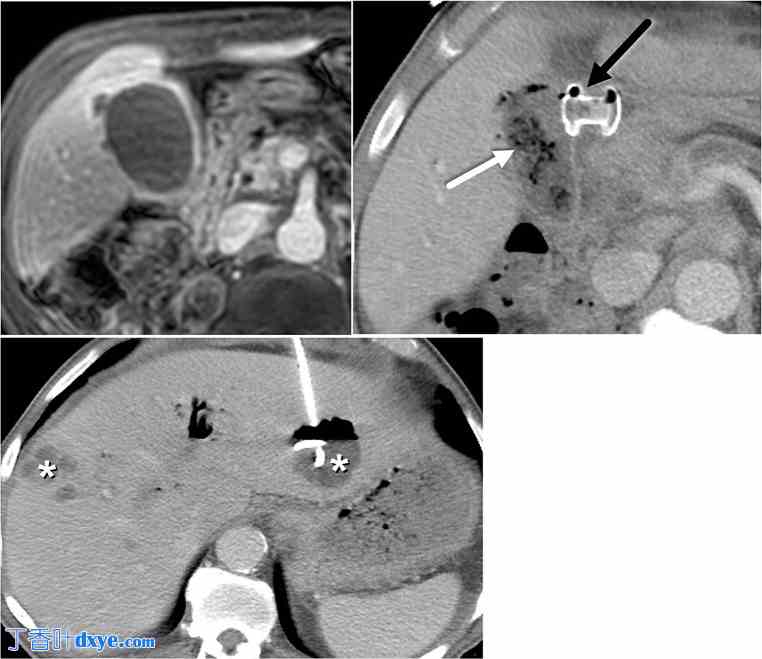
72 岁女性,患有胰腺颈癌和急性胆囊炎。A. 造影后轴向 LAVA MRI 显示胆囊壁不规则,局部外翻,表明胆囊壁穿孔(白色箭头)与坏疽性胆囊炎有关,这是内镜胆囊引流的禁忌症,但前瞻性地没有发现。B. 随后进行了 LAMS 胆囊胃造口术(黑色箭头)。注意到部分减压胆囊中预期有空气(白色箭头)。 C. 患者出现多个肝脓肿(白色星号),需要经皮引流,最终死于脓毒症
内镜超声引导胆道引流(EUS-BD),例如 EUS 引导胆总管十二指肠造口术(EUS-CD),涉及从十二指肠到胆管的解剖外支架置入,已成为 PTBD 的可行选择,临床成功率高,复发率低(图 6)。
图 6。
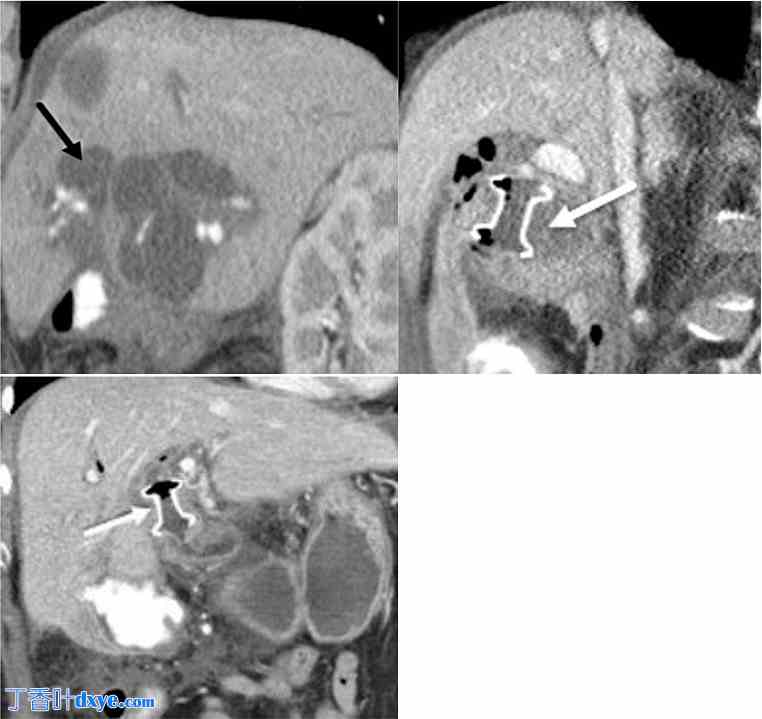
63 岁女性,胰头腺癌较大,阻塞了胆总管,无法通过经乳头入路置入支架。A. 增强矢状面 CT 图像显示严重的肝内胆管扩张(黑色箭头)。B 和 C. 增强矢状面 (B) 和冠状面 (C) CT 图像显示 LAMS(白色箭头)位于十二指肠球和近端胆总管之间,肝内胆管扩张已消退,预计会出现胆道积气
图 7。
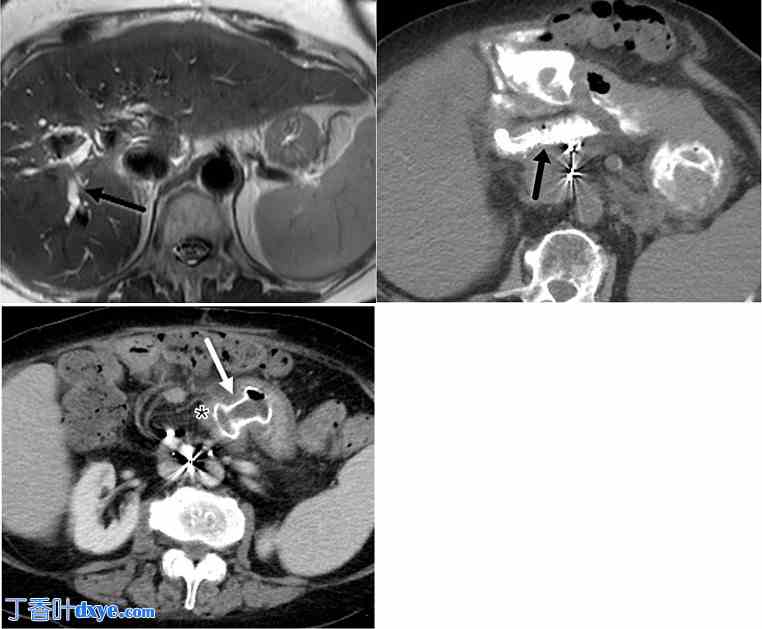
76 岁女性,曾接受过恶性 IPMN 的 Whipple 手术,在化疗和放疗后出现胆道狭窄。由于胆道狭窄和胆管炎具有复发性,患者每几个月需要接受一次 ERCP 来治疗胆道狭窄扩张,这在技术上具有挑战性。A. 轴向 T2 加权 MRI 显示肝内胆道扩张(黑色箭头),需要每 2-3 个月重复扩张狭窄并频繁更换支架。由于 Whipple 手术后解剖结构发生了改变,频繁进行 ERCP 在技术上具有挑战性。拟议的干预措施包括在残胃和胰胆管肢之间建立一条穿过胃空肠造口术的永久导管,以便于通过内窥镜进入胆道扩张/引流。B. 为了促进 LAMS 穿过胃空肠造口术,在部署 LAMS 之前,必须通过经皮经肝胆管造影通过肝空肠造口术引入造影剂来扩张胰胆管肢。此轴向 CT 图像显示造影剂使胰胆管扩张(黑色箭头)。C. 造影剂增强轴向 CT 证实 LAMS(白色箭头)已成功置于胃和胰胆管(星号)之间,从而为 ERCP 通路创建永久留置导管
图 8。
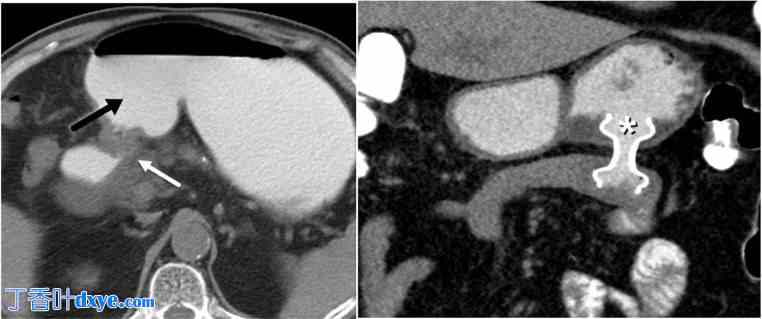
83 岁男性,胰腺癌患者,接受姑息性内镜胃空肠造口术。A. 造影剂增强轴向 CT 图像显示部分胃出口阻塞,由于已知幽门和十二指肠第一部分存在胰腺癌(白色箭头),胃膨胀,充满口服造影剂(黑色箭头)。B. 造影剂增强冠状 CT 图像显示通过 LAMS 进行姑息性胃空肠造口术(白色星号),显示管腔通畅,可缓解阻塞并避免手术
图 9。
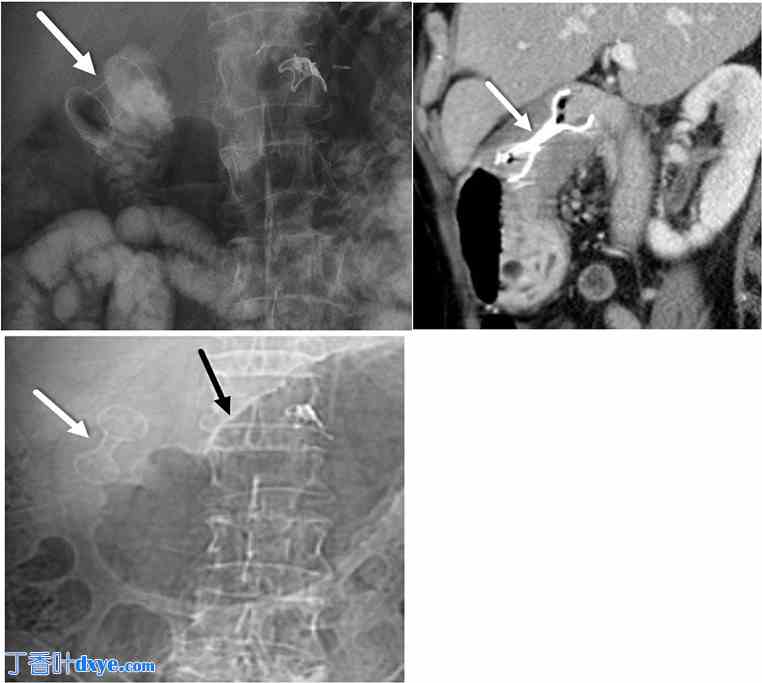
63 岁患者,因消化性溃疡病导致胃出口综合征而出现良性幽门狭窄。A. 腹部 X 光片显示腔内 LAMS(白色箭头),用于缓解良性幽门狭窄,临床症状明显改善。B. 一年后,患者失访后返回时获得的增强矢状 CT 图像显示,由于放置在幽门上的 LAMS 粘膜内生长,导致新的管腔狭窄(白色箭头)。 C. 与患者同时获得的正面 CT 地形图显示 LAMS 管腔出现新的狭窄(白色箭头),这是由于粘膜内生和由此导致的复发性胃出口梗阻(胃扩张(黑色箭头))造成的并发症
图 10。
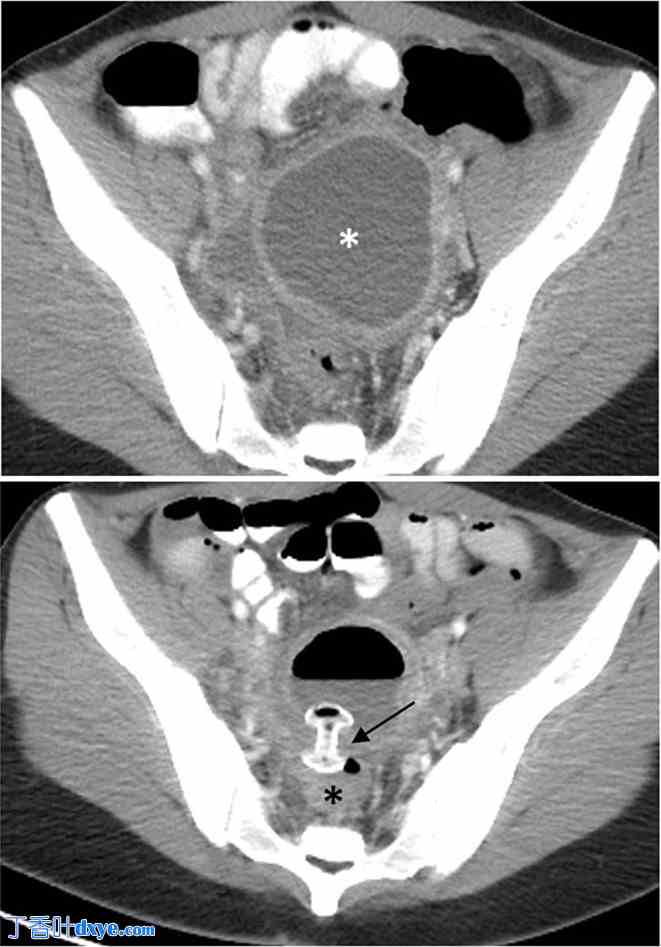
26 岁女性出现输卵管卵巢脓肿破裂,无法通过 IR 引流进入。A. 对比增强轴向 CT 图像显示输卵管卵巢脓肿破裂(白色星号)。B. 对比增强轴向 CT 图像显示通过 LAMS(黑色箭头)成功间歇性引流到直肠(黑色星号)
图 11。
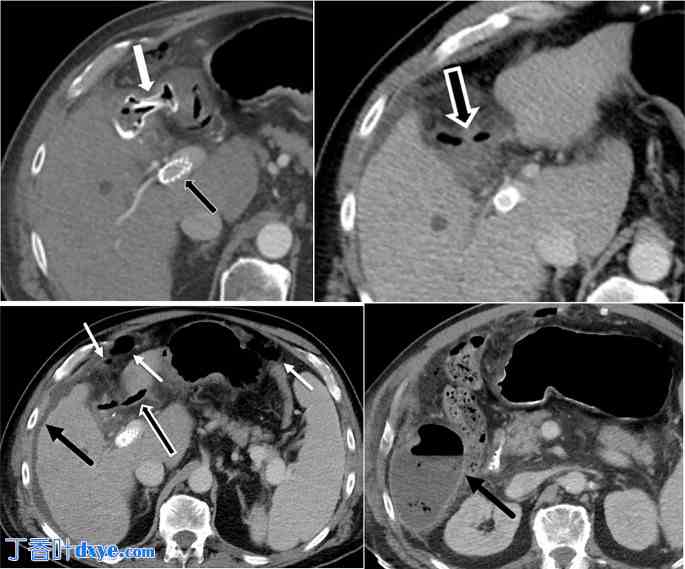
58 岁肝硬化男性患者,患有急性慢性胆囊炎,并发门脉高压症 s/p TIPS 手术。 A. 增强轴向 CT 图像显示 LAMS(白色箭头)位于胃和胆囊之间,猪尾导管穿过 LAMS 便于固定,并进行 TIPS(黑色箭头)。B. 一个月后,进行了间歇性腹腔镜胆囊切除术,并移除了 Axios 支架。增强轴向 CT 显示残留瘘管(黑色箭头)的可视化。C. 几天后,增强轴向 CT 显示持续性瘘管(黑色箭头轮廓)导致上腹部和中腹部积聚自由空气(白色箭头)和液体(黑色箭头)。 D. 三周后,增强轴向 CT 图像显示右侧肝下脓肿间隔发展(黑色箭头)
图 12。
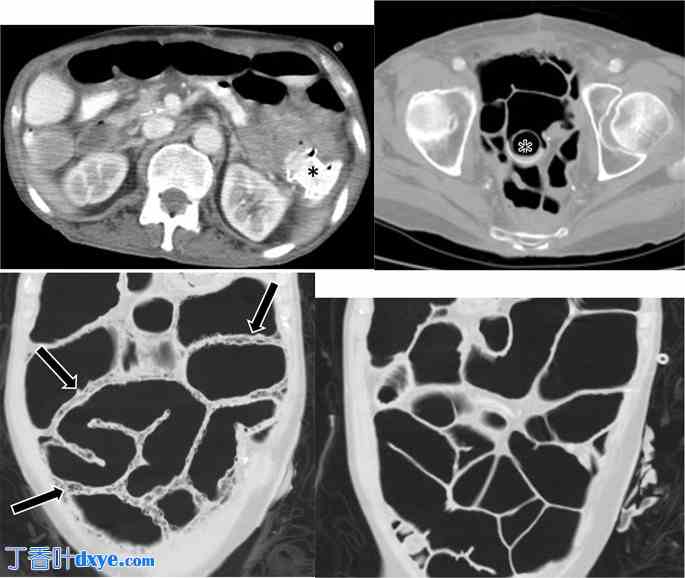
58 岁男性,有远端直肠癌病史,曾接受过腹会阴切除术,随后因局部复发而接受盆腔廓清术。患者病程因空盆综合征和复发性盆腔疾病导致的慢性小肠梗阻而变得复杂。通过结肠造口术将 LAMS 置于小肠和降结肠之间,以便进行旁路和减压。A. 增强轴向 CT 显示 LAMS(黑色星号)位于左上象限,连接空肠和降结肠。B. 三个月后的增强轴向 CT 显示移位的 LAMS(黑色星号),现在在盆腔远端小肠中可见。 C. 冠状 CT 图像显示新的、广泛的肠壁积气(黑色箭头)和小肠扩张。患者相对无症状,实验室检查未发现感染或缺血迹象。一个可能的假设是 LAMS 移位可能导致肠结肠瘘,导致肠内气体逸出/解剖到肠壁。D. 更换 LAMS 三周后获得的冠状 CT 图像显示肠壁积气完全消退 |


